题目内容
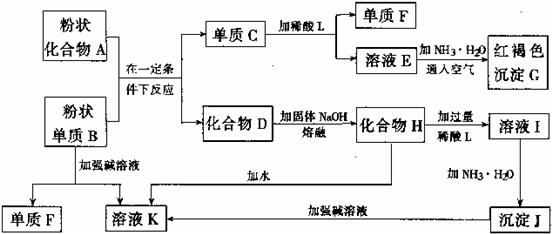
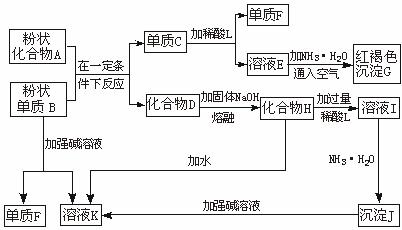
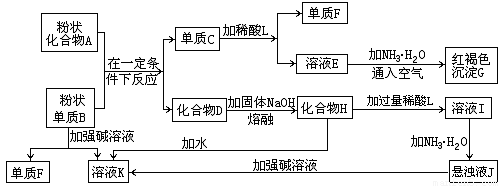
某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
(1)单质F是__________________________。
(2)写出由E生成G的离子反应方程式(或化学方程式)__________________________。
(3)溶液I中所含金属离子是_________________。
(4)由C→E+F一步反应所加的酸,不能选用的是(写化学式)___________或__________。
(1)H2 (2)4Fe2++8NH3·H2O+O2+2H2O====4Fe(OH)3↓+8 (3)Al3+和Na+ (4)H2SO4 HNO3 解析:由题G为红褐色沉淀可知G为Fe(OH)3,即框图中含Fe元素;再从溶液I加氨水得到的沉淀J可溶于强碱溶液,说明J为Al(OH)3,即框图中含Al元素。因此此题重点考查Al、Fe知识体系的掌握程度,特别是铝的两性、铁的可变化合价。两种元素间的重要反应是铝热反应。据此,结合A、B、C、D间的转化关系可知A+BC+D为铝热反应,其中C为Fe,D为Al2O3,由此可得出此题的正确答案。 由于Fe和浓H2SO4、HNO3反应不生成H2,故L不能是浓H2SO4或HNO3。![]() 或Fe2++2NH3·H2O====Fe(OH)2↓+2
或Fe2++2NH3·H2O====Fe(OH)2↓+2![]() ,4Fe(OH)2+O2+2H2O====4Fe(OH)3
,4Fe(OH)2+O2+2H2O====4Fe(OH)3
尖子生学案系列答案
满分训练设计系列答案

期末冲刺100分完全试卷系列答案
夺冠单元检测卷系列答案
全能测控课堂练习系列答案
一本好卷系列答案
单元考王系列答案
1加1轻巧夺冠优化训练系列答案
启东黄冈作业本系列答案