题目内容
【题目】下列反应的离子方程式正确的是
A. 钠与水反应:2Na +2H2O = 2Na++2OH-+H2↑
B. 氯气通入水中:Cl2 +H2O= 2H++ClO-+Cl-
C. 硫酸溶液与氢氧化钡溶液:H+ + SO42- + Ba2++ OH-=BaSO4↓ + H2O
D. Na2O 加入稀硫酸中:O2-+2H+ = H2O
【答案】A
【解析】
钠与水反应生成氢氧化钠和氢气;次氯酸是弱电解质,离子方程式中不能拆写成离子;H2SO4溶液与Ba(OH)2溶液反应生成硫酸钡和水的物质的量比为1:2;氧化物在离子方程式中不能拆写成离子;
钠与水反应生成氢氧化钠和氢气,反应离子方程式是2Na +2H2O = 2Na++2OH-+H2↑,故A正确;次氯酸是弱电解质,氯气通入水中的离子方程式是Cl2 +H2O= H++Cl-+HClO,故B错误 ;H2SO4溶液与Ba(OH)2溶液反应的离子方程式是2H++ SO42-+Ba2++2OH![]() BaSO4↓+2H2O,故C错误;Na2O 加入稀硫酸中生成硫酸钠和水,反应的离子方程式是:Na2O+2H+ = 2Na ++H2O,故D错误。
BaSO4↓+2H2O,故C错误;Na2O 加入稀硫酸中生成硫酸钠和水,反应的离子方程式是:Na2O+2H+ = 2Na ++H2O,故D错误。

练习册系列答案
相关题目
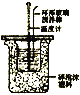
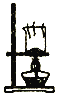
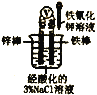
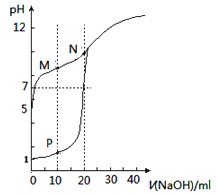
【题目】下列图示装置和对应实验原理的描述均正确的是
A | B | C | D |
|
|
|
|
根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 加热固体NaHCO3制备少量的Na2CO3 | 验证牺牲阳极的阴极保护法,可证明铁被保护 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 |
A. AB. BC. CD. D