题目内容
8.下列方法不能区分乙醇和乙酸的是( )| A. | 滴加酚酞溶液 | B. | 加入氧化钠 | ||
| C. | 滴加紫色石蕊溶液 | D. | 滴加碳酸钠溶液 |
分析 乙醇和乙酸都溶于水,乙酸含有羧基,具有酸性,结合性质的不同进行鉴别.
解答 解:A.乙醇与乙酸中滴加酚酞,均为无色,现象相同,不能鉴别,故A选;
B.氧化钠与乙醇不反应,与乙酸发生反应,固体溶解,现象不同,能鉴别,故B不选;
B.乙醇中滴加石蕊为紫色,乙酸中滴加石蕊变为红色,现象不同,能鉴别,故C不选;
D.乙酸与碳酸钠溶液反应生成二氧化碳气体,乙醇不能,可鉴别,故D不选;
故选A.
点评 本题考查有机物的鉴别,为高频考点,把握有机物的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意现象相同不能鉴别物质,题目难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
19.一定温度下的恒容密闭容器中,反应A2(g)+B2(g)?2AB(g) 达到平衡的标志是( )
| A. | 容器内n(A2):n(B2):n(AB)=1:1:2 | |
| B. | 单位时间内生成2nmolAB,同时生成nmolA2 | |
| C. | 生成B的速率与生成A的速率相等 | |
| D. | 容器内气体的密度不随时间变化 |
3.下列反应中,属于加成反应的是( )
| A. | CH3CH=CH2+Br2→CH3CHBrCH2Br | |
| B. | CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2+H2O | |
| C. | CH3COOH+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| D. | C6H6+HNO3$→_{△}^{浓H_{2}SO_{4}}$C6H5NO2+H2O |
13.以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

(1)滤液P中含有的阳离子有H+、Fe2+、Mg2+.
(2)过程Ⅱ中发生的氧化还原反应的离子方程式是2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)已知:
过程Ⅲ中加入NH3•H2O调节溶液pH约为4,其目的是使Fe3+沉淀完全而Mg2+不沉淀.
(4)过程Ⅳ在800℃煅烧MgSO4,发生多个反应,产物除MgO外,还有SO2、CO2、CO、S等气体产物,利用右图装置判断煅烧产生的气体.
①A中试管壁附着有淡黄色固体,该固体的化学式是S.
②B中盛放的溶液是(填字母)d.
a.NaOH 溶液 b.Na2CO3 溶液
c.稀硝酸 d.KMnO4溶液
③写出800℃煅烧MgSO4,产生气体产物是S 和CO的化学方程式MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑.

(1)滤液P中含有的阳离子有H+、Fe2+、Mg2+.
(2)过程Ⅱ中发生的氧化还原反应的离子方程式是2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)已知:
| Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | |
| 开始沉淀的pH | 10.4 | 1.9 | 7.0 |
| 沉淀完全的pH | 12.4 | 3.2 | 9.0 |
(4)过程Ⅳ在800℃煅烧MgSO4,发生多个反应,产物除MgO外,还有SO2、CO2、CO、S等气体产物,利用右图装置判断煅烧产生的气体.
①A中试管壁附着有淡黄色固体,该固体的化学式是S.
②B中盛放的溶液是(填字母)d.
a.NaOH 溶液 b.Na2CO3 溶液
c.稀硝酸 d.KMnO4溶液
③写出800℃煅烧MgSO4,产生气体产物是S 和CO的化学方程式MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑.
17.下列表述正确的是( )
| A. | 已知常温下0.1mol•L-1NaHA溶液的pH=9,则:c(Na+)═c(A2-)+c(HA-)+c(H2A) | |
| B. | 等pH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH${\;}_{4}^{+}$)=c(K+)=c(Ba2+) | |
| C. | 25℃,pH=12的氨水和pH=2的盐酸等体积混合:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| D. | 向AgNO3溶液中先滴加NaCl溶液至不再有沉淀生成,继续滴加Na2S溶液,观察到白色沉淀转化为黑色,则溶解度大小关系为:Ag2S>AgCl |
18.在一定条件下,对于密闭容器中进行的可逆反应:N2(g)+3H2(g)?2NH3(g).下列说法中,表明这一反应已经达到化学平衡状态的是( )
| A. | N2、H2、NH3的浓度不再变化 | B. | N2、H2、NH3的浓度为1﹕3﹕2 | ||
| C. | N2、H2、NH3在密闭容器中共存 | D. | 反应停止,正、逆反应速率都等于0 |
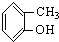 酚
酚 酮
酮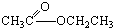 酯
酯 醛
醛 酸.
酸.

 命名为2-甲基-1,3-丁二烯.
命名为2-甲基-1,3-丁二烯.