题目内容
下列叙述中正确的是
| A.酚类中加入浓溴水一定能产生白色沉淀 |
| B.氮化硅陶瓷属于无机非金属材料 |
| C.浓硝酸存放于带橡胶塞的棕色细口瓶中 |
| D.淀粉和纤维素的分子式都是(C6H10O5)n |
B
试题分析:A. 不一定会有白色沉淀,酚羟基的邻位和对位没有氢原子可取代时,即是不能被溴取代;B.氮化硅陶瓷从元素的角度属于非金属材料,正确;C.浓硝酸会氧化橡胶,应用玻璃塞,错误;D.淀粉和纤维素不能讲分子式为(C6H10O5)n,因为它们的n值不一样,只能说通式。

练习册系列答案
相关题目
 Si(粗)+2CO
Si(粗)+2CO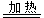 SiCl4
SiCl4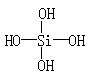 , 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为( )
, 则在所得的H6Si2O7分子的结构中,含有的硅氧键数目为( )  CuSO4 +SO2↑+2H2O
CuSO4 +SO2↑+2H2O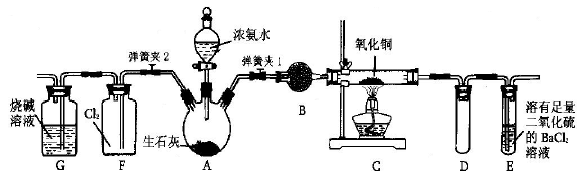
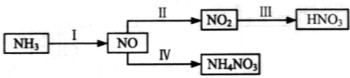
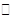 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。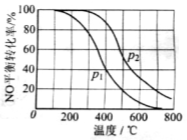
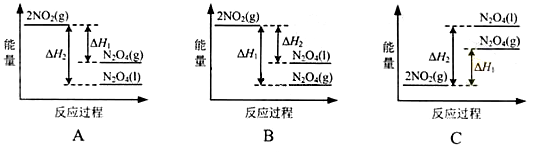
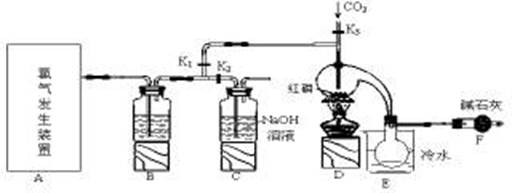
 a.用干燥洁净的烧杯取约10 mL浓硝酸,加热。
a.用干燥洁净的烧杯取约10 mL浓硝酸,加热。