题目内容
(15分)
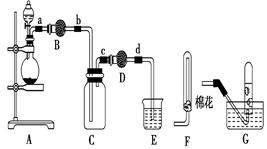
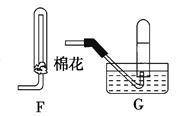
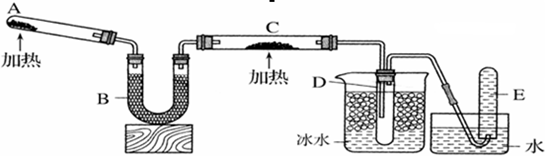
三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如下图所示。
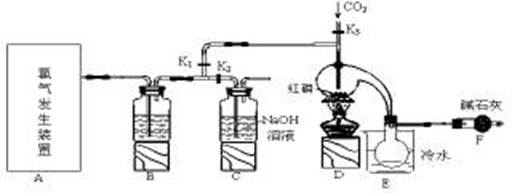
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷), POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
请回答:
(1)写出A中反应的离子方程式 。
(2)B装置中所盛试剂是 ;E中烧杯内冷水的作用是 。
(3)实验前玻璃管之间连接需要用到橡皮管,其连接方法是:先把 ,然后稍稍用力即可把玻璃管插入橡皮管中。
(4)检查装置气密性后,向D装置的曲颈瓶中加入红磷,打开K3通入干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。其中通入干燥CO2的目的是 。
(5)实验制得的粗产品中常含有POCl3、PCl5等,加入红磷加热除去PCl5后,再通过 (填实验名称)即可得到较纯净的PCl3。
(6)实验后关闭K1,打开K2,将A、B中余氯通入300ml 1mol/L的NaOH溶液中。若NaOH恰好完全反应,则吸收氯气的物质的量为(假设反应生成了NaCl 、 NaClO 和 NaClO3等钠盐) mol,反应中转移电子的物质的量(n)的范围是 。
三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如下图所示。

已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷), POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)写出A中反应的离子方程式 。
(2)B装置中所盛试剂是 ;E中烧杯内冷水的作用是 。
(3)实验前玻璃管之间连接需要用到橡皮管,其连接方法是:先把 ,然后稍稍用力即可把玻璃管插入橡皮管中。
(4)检查装置气密性后,向D装置的曲颈瓶中加入红磷,打开K3通入干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。其中通入干燥CO2的目的是 。
(5)实验制得的粗产品中常含有POCl3、PCl5等,加入红磷加热除去PCl5后,再通过 (填实验名称)即可得到较纯净的PCl3。
(6)实验后关闭K1,打开K2,将A、B中余氯通入300ml 1mol/L的NaOH溶液中。若NaOH恰好完全反应,则吸收氯气的物质的量为(假设反应生成了NaCl 、 NaClO 和 NaClO3等钠盐) mol,反应中转移电子的物质的量(n)的范围是 。
(除标注外,每空2分,共15分)
(1) MnO2 + 4H+ + 2Cl—△ Mn2+ + Cl2↑+ 2H2O (其他合理答案均计分)
(2) 浓硫酸 冷凝,便于收集产品 (合理答案均计分)
(3) 玻璃管口用水润湿(合理答案均计分)
(4) 排尽曲颈瓶中的空气,防止PCl3与O2等发生副反应(合理答案均计分)
(5) 蒸馏
(6) 0.15 (1分) 0.15mol < n < 0.25mol (无单位此次不扣分)
(1) MnO2 + 4H+ + 2Cl—△ Mn2+ + Cl2↑+ 2H2O (其他合理答案均计分)
(2) 浓硫酸 冷凝,便于收集产品 (合理答案均计分)
(3) 玻璃管口用水润湿(合理答案均计分)
(4) 排尽曲颈瓶中的空气,防止PCl3与O2等发生副反应(合理答案均计分)
(5) 蒸馏
(6) 0.15 (1分) 0.15mol < n < 0.25mol (无单位此次不扣分)
试题分析:(1)A装置是产生氯气的装置,二氧化锰与浓盐酸加热制取氯气,离子方程式为 MnO2 + 4H+ + 2Cl—△ Mn2+ + Cl2↑+ 2H2O ,或者用高锰酸钾溶液与浓盐酸不加热制取氯气;
(2)实验室常用红磷与干燥的Cl2制取PCl3,所以氯气需干燥后通入C中,B中盛放浓硫酸;PCl3的熔点较低,所以E中烧杯内冷水的作用是 冷凝,便于收集产品 ;
(3)玻璃管与橡胶管连接时,往往把胶管的一端用水浸湿,或把玻璃管口用水润湿,方便连接;
(4)因为PCl3遇O2会生成POCl3,所以装置内不能存在氧气,所以通入干燥CO2的目的排尽曲颈瓶中的空气,防止PCl3与O2等发生副反应生成POCl3;
(5)由信息可知,POCl3与PCl3都是液体,沸点相差较大,故可以用蒸馏的方法进行分离;
(6)300ml 1mol/L的NaOH溶液中Na元素的物质的量是0.3mol,根据元素守恒,生成的NaCl 、 NaClO 和 NaClO3等钠盐的总物质的量为0.3mol,所以需要氯气0.15mol;若只生成NaCl 、 NaClO ,则转移的电子最少为0.15mol×2×1/2=0.15mol,若只生成NaCl 、 NaClO3,则转移的电子最多,根据得失电子守恒,NaCl 、 NaClO3的物质的量之比是5:1,所以转移电子的物质的量为0.15mol×2×5/6=0.25mol,当三种产物都存在时转移电子的物质的量介于二者之间 0.15mol < n < 0.25mol 。

练习册系列答案
相关题目
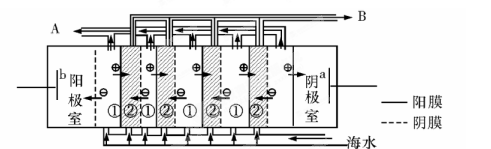
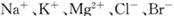 等离子)可提取溴,其生产流程如下:
等离子)可提取溴,其生产流程如下: