��Ŀ����
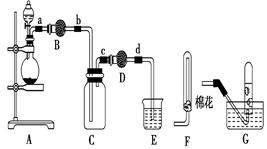
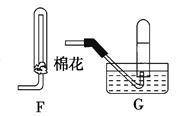
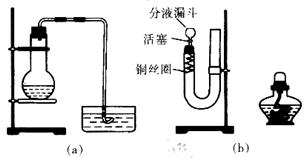
��ͼ��ʾ����ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������
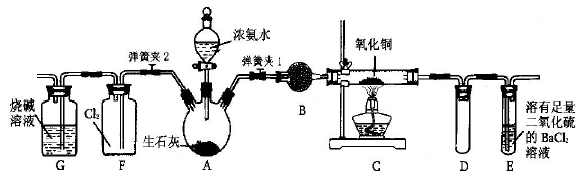
��l��д��װ��A���������Ļ�ѧ��Ӧ
��2��װ��B��ʢ���Լ���
��3����ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©�����Ժ�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ��
�� ����д��Ӧ������E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ
��4����֪Cu2O��һ�ֺ�ɫ��������, �ڸ��������¿���CuO�ֽ�õ���4CuO��2Cu2O+O2�������ɵ�Cu2O Ҳ�ܱ�NH3��ԭ����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16g����Ӧ����ع�����������2��4g��ͨ������ȷ���ù������ijɷ��� ���û�ѧʽ��ʾ��
��5���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�С�д���������̵Ļ�ѧ����ʽ

��l��д��װ��A���������Ļ�ѧ��Ӧ
��2��װ��B��ʢ���Լ���
��3����ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©�����Ժ�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ��
�� ����д��Ӧ������E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ
��4����֪Cu2O��һ�ֺ�ɫ��������, �ڸ��������¿���CuO�ֽ�õ���4CuO��2Cu2O+O2�������ɵ�Cu2O Ҳ�ܱ�NH3��ԭ����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16g����Ӧ����ع�����������2��4g��ͨ������ȷ���ù������ijɷ��� ���û�ѧʽ��ʾ��
��5���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�С�д���������̵Ļ�ѧ����ʽ
��1��NH3��H2O��CaO�� Ca(OH)2 + NH3 �� ��2����ʯ�һ���ʯ��
��3����ɫ������2NH3��3CuO 3Cu+N2����3H2O ��4��Cu2O��Cu
3Cu+N2����3H2O ��4��Cu2O��Cu
��5��3Cl2��8NH3��N2��6NH4Cl
��3����ɫ������2NH3��3CuO
 3Cu+N2����3H2O ��4��Cu2O��Cu
3Cu+N2����3H2O ��4��Cu2O��Cu��5��3Cl2��8NH3��N2��6NH4Cl
�����������l��װ��AΪ�����ķ���װ�ã�����Ũ��ˮ����ʯ�ҷ�Ӧ�����������ƺͰ����������Ļ�ѧ��ӦΪNH3��H2O��CaO�� Ca(OH)2 + NH3 ������2��װ��BΪ�����ĸ���װ�ã�ʢ���Լ��Ǽ�ʯ�һ���ʯ�ң� ��3��װ��E������Ϊ��ȥ�����İ����������ķ�ӦΪSO2+2NH3��H2O����NH4��2SO3+H2O��
��NH4��2SO3+BaCl2
 Ba SO3+ NH4Cl��װ��E�е�����Ϊ����Һ����ִ������ݣ�ͬʱ������ɫ��������������֪��װ��C�з����ķ�ӦΪ����������ͭ�ڼ��������·�Ӧ����ͭ��������ˮ����ѧ����ʽΪ2NH3��3CuO
Ba SO3+ NH4Cl��װ��E�е�����Ϊ����Һ����ִ������ݣ�ͬʱ������ɫ��������������֪��װ��C�з����ķ�ӦΪ����������ͭ�ڼ��������·�Ӧ����ͭ��������ˮ����ѧ����ʽΪ2NH3��3CuO 3Cu+N2����3H2O����4��16gCuO�к���ͭԪ������Ϊ16g��64/80=12.8g��������Ԫ������Ϊ16g-12.8g=3.2g����Ӧ����ع�����������2.4g��ʣ���������Ϊ16g-2.4g=13.6g������12.8g����ʣ����庬��Cu��OԪ�أ�n��Cu��=0.2mol��������Ԫ�ص�����Ϊ13.6g-12.8g=0.8g��n��O��=0.05mol��n��Cu����n��O��=0.2mol��0.05mol=4��1��2��1��ʣ�����ΪCu2O��Cu����5���ڹرյ��ɼ�1���ɼ�2�������������F�У�װ��F�в������̣������ķ�ӦΪ3Cl2��8NH3��N2��6NH4Cl��
3Cu+N2����3H2O����4��16gCuO�к���ͭԪ������Ϊ16g��64/80=12.8g��������Ԫ������Ϊ16g-12.8g=3.2g����Ӧ����ع�����������2.4g��ʣ���������Ϊ16g-2.4g=13.6g������12.8g����ʣ����庬��Cu��OԪ�أ�n��Cu��=0.2mol��������Ԫ�ص�����Ϊ13.6g-12.8g=0.8g��n��O��=0.05mol��n��Cu����n��O��=0.2mol��0.05mol=4��1��2��1��ʣ�����ΪCu2O��Cu����5���ڹرյ��ɼ�1���ɼ�2�������������F�У�װ��F�в������̣������ķ�ӦΪ3Cl2��8NH3��N2��6NH4Cl��
��ϰ��ϵ�д�
 ��һ������Ԫͬ�����ؾ�ϵ�д�
��һ������Ԫͬ�����ؾ�ϵ�д�
�����Ŀ
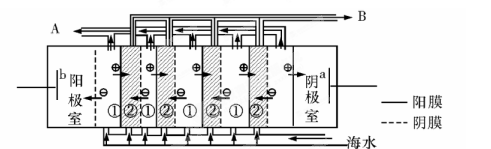
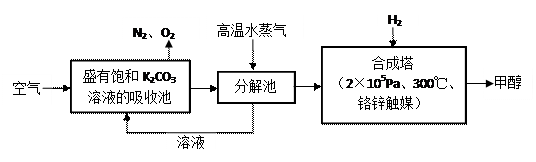 ������п�ѧ���������ɫ���ɡ����룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ֮��Ϊ������ȼ�ϼ״�������ɫ���ɡ����뼼���������£�
������п�ѧ���������ɫ���ɡ����룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ֮��Ϊ������ȼ�ϼ״�������ɫ���ɡ����뼼���������£�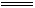 2Na2SO4+O2��+2H2O+2CO2��
2Na2SO4+O2��+2H2O+2CO2��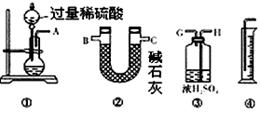
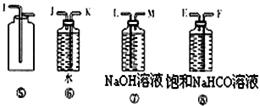
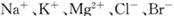 �����ӣ�����ȡ�壬�������������£�
�����ӣ�����ȡ�壬�������������£�