题目内容
【题目】二氧化氯(ClO2)是一种优良的消毒剂,熔点为-59℃,沸点为 11℃,浓度过高时易发生分解,甚至爆炸。某课外兴趣小组通过氯气与 NaClO2溶液反应来制取少量ClO2,装置如下图所示:
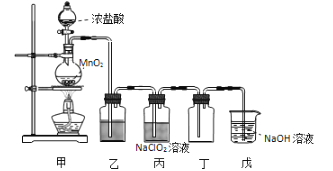
(1)甲装置中圆底烧瓶内发生反应的化学方程式是____________________。
(2)丙装置中发生的反应可能经两步完成,请将其补充完整:
①____________________________________________(用化学方程式表示),
②HClO + HCl + 2NaClO2 2ClO2↑+ 2NaCl + H2O。
(3)Clˉ存在时会催化 ClO2的生成,若无乙装置,则丙装置内产生 ClO2的速率明显加快。乙装置中试剂瓶内的液体是__________。实验过程中常需通入适量的 N2稀释 ClO2,其目的是_______________________。
(4)戊装置烧杯中 NaOH 溶液吸收 ClO2后,生成了 ClO2-、ClO3-,该反应的离子方程式是__________。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O Cl2+H2O
MnCl2+Cl2↑+2H2O Cl2+H2O![]() HCl+HClO 饱和食盐水 防止ClO2 发生分解,甚至爆炸 2ClO2+2OH-= ClO2- +ClO3- +H2O
HCl+HClO 饱和食盐水 防止ClO2 发生分解,甚至爆炸 2ClO2+2OH-= ClO2- +ClO3- +H2O
【解析】
(1)甲装置中是MnO2和HCl(浓)反应制氯气的。
(2)丙装置中氯气先和水反应,反应的化学方程式为Cl2+H2O![]() HCl+HClO。
HCl+HClO。
(3)从甲装置中出来的氯气中混有氯化氢,氯气在饱和食盐水中不溶,氯化氢溶解在水中。
(4)根据元素守恒和电荷守恒配平离子方程式。
(1)甲装置中是MnO2和HCl(浓)反应制氯气的,圆底烧瓶内发生反应的化学方程式是:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)丙装置中氯气先和水反应,反应的化学方程式为Cl2+H2O![]() HCl+HClO,故答案为:Cl2+H2O
HCl+HClO,故答案为:Cl2+H2O![]() HCl+HClO。
HCl+HClO。
(3)从甲装置中出来的氯气中混有氯化氢,氯气在饱和食盐水中不溶,氯化氢溶解在水中,故乙装置中试剂瓶内的液体是饱和食盐水,通入适量的 N2稀释 ClO2,其目的是防止ClO2 发生分解,甚至爆炸,故答案为:饱和食盐水;防止ClO2 发生分解,甚至爆炸。
(4)戊装置烧杯中NaOH溶液吸收 ClO2后,生成了 ClO2-、ClO3-,根据元素守恒可知产物还有水生成,再根据电荷守恒可得出该反应的离子方程式是:2ClO2+2OH-= ClO2- +ClO3- +H2O,故答案为:2ClO2+2OH-= ClO2- +ClO3- +H2O。