题目内容
在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ |
B
解析试题分析:A.发生反应:2Fe3++2I-=2Fe2++I2.不能共存。错误。B. pH值为1的溶液是酸性溶液,此时H+和Cu2+、Na+、Mg2+、NO3-不会发生任何反应。可以共存。正确。C. 在室温下纯水电离出来的c(H+)= 10-7mol/L.现在溶液中水电离出来的c(H+)=10-13mol/L<10-7 mol/L,说明水的电离受到了抑制,可能外加了酸或碱。在酸性溶液中H++HCO3-=H2O+CO2↑;在碱性溶液在OH-+HCO3-=H2O+CO32-。可见无论是酸性还是碱性都不能大量共存。错误。D.发生反应:3CO32-+2Al3+ +3H2O=2Al(OH)3↓+3CO2↑.不能大量共存。错误。
考点:考查离子共存的知识。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。
下列说法正确的是
| A.a点对应的溶液中大量存在:Al3+、Na+、Cl-、NO3- |
| B.b点对应的溶液中大量存在:K+、Ba2+、NO3-、I- |
| C.c点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- |
| D.d点对应的溶液中大量存在:Na+、K+、SO32-、Cl- |
常温下,下列各组离子能大量共存的是
| A.pH=12的溶液中:K+、Na+、Br-、AlO2- |
| B.无色溶液中:H+、K+、MnO4-、C2O42- |
| C.c(Fe3+)="0.1" mol·L-1的溶液中:K+、H+、SCN-、I- |
| D.由水电离出的c(OH-) =1.0×10-13 mol·L-1的溶液中:Na+、NH4+、SO42-、HCO3- |
下列化学方程式中,能用离子方程式:Ba2++SO42-=BaSO4↓表示的是
| A.Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3?H2O |
| B.Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C.BaCO3+H2SO4=BaSO4↓+2H2O+CO2↑ |
| D.BaCl2+ Na2SO4=BaSO4↓+2NaCl |
某强碱性溶液中含有的离子是:K+、NH4+、A13+、AlO2-、CO32-、SiO32-、Cl-中的某几种,现进行如下实验:
①取少量的溶液用足量硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加人盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失。
③另取一定量的原溶液中加人5 mL0. 2 mol/L盐酸时,沉淀会完全消失,加人足量的硝酸银溶液可得到沉淀0.187 g。下列说法中正确的是 ( )
| A.该溶液中一定不含NH4+、A13+、SiO32-、Cl- |
| B.该溶液中一定含有A13+、CO32-、Cl- |
| C.Cl-可能含有 |
| D.该溶液中一定含有AlO2-、CO32-、Cl- |
在pH=1的无色溶液中,下列离子能大量共存的是
| A.NH4+、Ba2+、NO3—、CO32— | B.K+、Mg2+、NO3-、SO42— |
| C.Fe2+、OH—、SO42—、MnO4— | D.Na+、Fe3+、Cl—、AlO2— |
下列表述正确的是
A.含有大量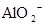 的溶液中:K+、 的溶液中:K+、 、 、 、 、 可共存 可共存 |
B.CO(g)的燃烧热是283.0kJ·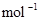 ,则 ,则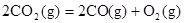 反应的 反应的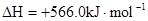 |
C.将SO2通入 溶液中: 溶液中: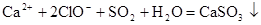 +2HClO +2HClO |
D.在某钠盐溶液中含有等物质的量的 、 、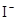 、 、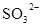 、 、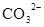 、 、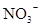 、 、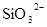 中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有 中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有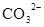 |
下列各组离子中,能在溶液中大量共存的是
| A.OH-Na+HCO3- Cl- | B.Ba2+ Na+Cl-SO42- |
| C.K+ Al3+ SO42-OH- | D.Ag+Al3+ NO3- H+ |
下列表示对应化学反应的离子方程式正确的是
| A.用白醋除铁锈:Fe2O3+6H+=3H2O+2Fe3+ |
| B.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热: Ba2++ 2OH-+NH4++ HCO3-  NH3↑+2H2O+BaCO3↓ NH3↑+2H2O+BaCO3↓ |
| C.用过量冷氨水吸收SO2:SO2+NH3·H2O=HSO3-+NH4+ |
| D.用强碱吸收工业制取硝酸尾气:NO+ NO2+2OH-=2NO3-+H2O |