题目内容
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿(主要成份:CuO ZnO)的方案,实现废物综合利用,方案如下图所示。

请回答下列问题:
(1)操作1的名称是:
(2)向溶液A中加入Fe粉发生的主要的反应离子方程式为: 、 。
(3)向溶液B中加入物质X的目的是 ,物质X可用下列物质中的 。(填字母)
A.KMnO4 B.O2 C.H2O2 D.NaOH
(4)向溶液B中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(5)溶液D中主要溶质的化学式是 。
(6)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(1)过滤(2分)
(2)Fe + 2H+=Fe2+ + H2↑(2分 Fe + Cu2+=Fe2+ + Cu(2分)
(3)将Fe2+氧化成Fe3+,以便除去 (2分)B C (2分)
(4)3.2 <PH< 6.2(2分)
(5)(NH4)2SO4 (2分) (6)< (2分)
【解析】
试题分析:(1)操作1为固液分离操作,所以名称为过滤。
(2)氧化铜锌矿加入硫酸后,氧化物溶解生成Cu2+、Zn2+,同时为了使矿物充分溶解,加入的酸要过量,所以酸浸后的滤液为酸性溶液,再加入Fe粉,发生反应Fe + 2H+=Fe2+ + H2↑、 Fe + Cu2+=Fe2+ + Cu。
(3)因为得到的B溶液要析出沉淀Fe(OH)3 ,所以须把二价铁氧化为三价铁以便更好的除去,所以除了加碱性氨水溶液外,还应该加入氧化剂,并且不引入杂质,所以可以选择O2 、H2O2 ,故选BC。
(4)加入氨水主要是使Fe3+完全沉淀而不能使Zn2+沉淀,所以应该控制PH范围在3.2 <PH< 6.2之间
(5)由于过程中两次加入氨水,且C溶液中的Zn2+和碳酸根离子生成了沉淀碱式碳酸锌,所以剩余D溶液中含有的大量阳离子为NH4+,大量阴离子为SO42-,所以主要溶质为(NH4)2SO4 。
(6)在H2SO4的作用下ZnS可以溶解而CuS不溶,说明CuS更难溶,所以相同温度下,Ksp(CuS)<Ksp(ZnS)。
考点:本题考查的是化工流程题。


已知:各离子开始沉淀及完全沉淀时的pH如下表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)
(3)物质A最好使用下列物质中的
A.KMnO4 B.空气 C.HNO3 D.NaClO
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在
(5)物质B可直接用作氮肥,则B的化学式是
(6)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂--K2FeO4,写出该反应的离子方程式
(14分))某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如下图所示。

已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
|
离子 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe2+ |
6.34 |
9.7 |
|
Fe3+ |
1.48 |
3.2 |
|
Zn2+ |
6.2 |
8.0 |
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS
不溶,这是由于相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(2)你认为在除铁过程中选用下列物质中的 (填序号)作为试剂甲是比较合适的。
A.KMnO4 B.HNO3 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方程式 。
(5)298K时,残留在乙溶液中的c(Fe3+)在 __ mol/L以下。
[Fe(OH)3的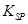 = 2.70×10-39]
= 2.70×10-39]
(6)乙的溶液可直接用作氮肥,则乙的化学式是 。
(7)请写出“沉淀Zn2+”步骤中发生反应的化学方程式 。

