��Ŀ����
��14�֣���ij����С����Ƴ����ù�ҵ���ᣨ10%H2SO4�����ѽ�ij����������ͭп����ȡ����ZnO�ķ�����ʵ�ַ����ۺ����ã���������ͼ��ʾ��

��֪��298Kʱ�����ӿ�ʼ��������ȫ����ʱ��pH���±���ʾ��
|
���� |
��ʼ����ʱ��pH |
��ȫ����ʱ��pH |
|
Fe2�� |
6��34 |
9��7 |
|
Fe3�� |
1��48 |
3��2 |
|
Zn2�� |
6��2 |
8��0 |
��ش��������⣺
��1������ͭп���к���������CuS��ZnS����H2SO4��������ZnS�����ܽ��CuS
���ܣ�����������ͬ�¶��£�Ksp��CuS�� Ksp��ZnS����ѡ�������������������
��2������Ϊ�ڳ���������ѡ�����������е� ������ţ���Ϊ�Լ����DZȽϺ��ʵġ�
A��KMnO4 B��HNO3 C��H2O2 D��Cl2
��3�����������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������ ��Χ֮�䡣
��4����д���Ӽ����ʺ��백ˮ���Ƶ�����Һ��pH������Fe��OH��3��Ӧ�����ӷ���ʽ ��
��5��298Kʱ������������Һ�е�c��Fe3������ __ mol/L���¡�
[Fe��OH��3��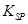 = 2��70��10-39]
= 2��70��10-39]
��6���ҵ���Һ��ֱ���������ʣ����ҵĻ�ѧʽ�� ��
��7����д��������Zn2+�������з�����Ӧ�Ļ�ѧ����ʽ ��
��1���� ��2��C ��3��3��2~6��2
��4��Fe3++3NH3��H2O === Fe��OH��3��+3 NH4+
��5��2��7��10-21
��6����NH4��2SO4
��7��2ZnSO4 +NH4HCO3 +3 NH3��H2O== Zn2��OH��2CO3 ��+2��NH4��2 SO4 + H2O
��������

 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�
��֪�������ӿ�ʼ��������ȫ����ʱ��pH���±���ʾ��
| ���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
��1���ڡ�����������У�Ϊ��߽������ʣ���ͨ����������衱�⣬���ɲ�ȡ�Ĵ�ʩ��
��2������ͭп���к���������CuS��ZnS����H2SO4��������ZnS�����ܽ��CuS���ܣ�����ͬ�¶��£�Ksp��CuS��
��3������A���ʹ�����������е�
A��KMnO4 B������ C��HNO3 D��NaClO
��4�����������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������
��5������B��ֱ���������ʣ���B�Ļ�ѧʽ��
��6��������õ���Fe��OH��3����KClO��Һ�ڼ��Ի������������õ�һ�ָ�Ч�Ķ��ˮ������--K2FeO4��д���÷�Ӧ�����ӷ���ʽ


