题目内容
水溶液的pH值最大( )
| A、NaHCO3 |
| B、KHSO4 |
| C、AlCl3 |
| D、HF |
考点:盐类水解的应用
专题:盐类的水解专题
分析:溶液的pH最大,说明溶液中氢氧根浓度最大,氢离子浓度最小,可以先判断溶液的酸碱性,溶液pH大小关系为:碱性溶液>中性溶液>酸性溶液,根据盐的水解原理、电解质的电离对各选项进行判断即可.
解答:
解:A.碳酸氢钠溶液为强碱弱酸盐,碳酸氢根离子水解,导致溶液显示碱性,溶液的pH>7;
B.硫酸氢钾为强电解质,在水中电离出钾离子、氢离子和硫酸根离子,所以硫酸氢钾溶液具有强酸性,溶液的pH<7;
C.氯化铝溶液为强酸弱碱盐,铝离子部分水解,溶液显示弱酸性,溶液的pH<7;
D.氟化氢为弱电解质,溶液中部分电离出氢离子,溶液显示酸性,溶液的pH<7,
根据以上分析可知,溶液的pH最大的是A,
故选A.
B.硫酸氢钾为强电解质,在水中电离出钾离子、氢离子和硫酸根离子,所以硫酸氢钾溶液具有强酸性,溶液的pH<7;
C.氯化铝溶液为强酸弱碱盐,铝离子部分水解,溶液显示弱酸性,溶液的pH<7;
D.氟化氢为弱电解质,溶液中部分电离出氢离子,溶液显示酸性,溶液的pH<7,
根据以上分析可知,溶液的pH最大的是A,
故选A.
点评:本题考查盐类水解原理及应用、强弱电解质的电离等知识,为高考高频考点,侧重于学生对化学基本反应原理和应用的考查,难度不大,注意把握盐类水解的规律.

练习册系列答案
相关题目
某固体化合物R不导电,但熔化或溶于水中能完全电离,下列关于R的叙述中正确的是( )
| A、R为非电解质 |
| B、R为强电解质 |
| C、R为弱电解质 |
| D、R为离子化合物 |
下列叙述正确的是( )
| A、糖类也叫碳水化合物 |
| B、凡是符合Cn(H2O)m通式的物质均可称为碳水化合物 |
| C、由于糖类的分子式可以用通式Cn(H2O)m来表示,所以在它们的分子中H和O的原子个数比一定等于2:1 |
| D、聚乙烯、葡萄糖都是高分子化合物 |
下面是生产生活中的常见有机物的分子式、结构(简)式或名称:下列有关说法正确的是( )
① ②
②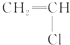 ③
③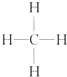 ④
④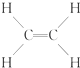 ⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
①
 ②
②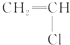 ③
③ ④
④ ⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.
⑤CH3CH2OH ⑥C6H12O6 ⑦CH3COOH ⑧硬脂酸甘油酯 ⑨蛋白质 ⑩聚乙烯.| A、能与溴的四氯化碳溶液发生加成反应并使之褪色的一定有①②④⑩ |
| B、投入钠一定能产生H2的是⑤⑦⑧⑨ |
| C、含碳量最高、有毒、常温下为液体且点燃时有浓的黑烟的是① |
| D、属于高分子材料的是⑧⑨⑩ |
盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表达不正确的是( )
| A、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- |
| B、NaHCO3溶液中:c(HCO3-)+c(H2CO3)+c(CO32-)=c( Na+) |
| C、相同温度下,l0mL 0.lmol?L-1的醋酸与100mL 0.01 mol?L-1的醋酸中H+的物质的量不相等 |
| D、相同温度下,中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH的物质的量,后者多 |
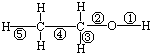 乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中不同的化学键如图.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A、与金属钠反应时,键①断裂 |
| B、在Ag催化下与O2反应时,键①、③断裂 |
| C、与CuO反应时,键①断裂 |
| D、与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂 |
意大利科学家使用氧分子和带正电的氧离子作用,合成出新型氧分子O4,反应过程可表示为:2O2
O4,下列说法错误的是( )
| ||
| A、O4与O2、O3都是氧的同素异形体 |
| B、合成O4属于物理变化 |
| C、O4与O2的化学性质完全相同 |
| D、O4的密度比O2大 |
把5molA和6molB的混合气体通入4L的密闭容器中,在一定条件下发生如下反应:5A(g)+4B(g)?6C(g)+xD(g),经过5min后反应达到平衡状态时,生成3mol C,并测得D的平均反应速率为0.1mol?L-1?min-1.下列计算结果正确的是( )
| A、x的数值是2 |
| B、A的转化率为40% |
| C、B的平衡浓度为4mol/L |
| D、反应前后混合气体的压强之比为22:23 |
氧化还原反应发生在同种元素之间的是( )
| A、Zn+2HCl═ZnCl2+H2↑ | ||||
| B、2H2S+SO2═3S+2H2O | ||||
| C、H2+CuO═Cu+H2O | ||||
D、2H2O
|