题目内容
下列说法正确的是( )
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH =" —40.69" kJ·mol-1 H2O(l) 的 ΔH =" —40.69" kJ·mol-1 |
| B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍 |
| C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH代表燃烧热 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
则可以计算出反应
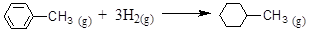 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1
A
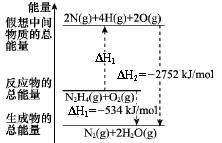
解析试题分析:A.气化热是1mol的物质在一定的条件下由液态变为气态所吸收的热量。在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则物质由气态转化为液态释放热量40.69 kJ。则H2O(g)  H2O(l) 的ΔH =" —40.69" kJ·mol-1。正确。B.燃烧热是1mol的物质完全燃烧产生稳定的氧化物时所释放的热量。在25℃、101kPa,2mol S的燃烧放出的热量是1mol S的燃烧放出热量2倍,但是燃烧热是相同的。错误。C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH并不代表燃烧热。因为水在气态时是不稳定的状态,液态才是水的稳定状态。错误。D.在苯分子中不含C-C及C=C,而是存在一种介于单键与双键之间的一种特殊的化学键。因此根据表格提供的数据不能计算出该反应的反应热。正确。
H2O(l) 的ΔH =" —40.69" kJ·mol-1。正确。B.燃烧热是1mol的物质完全燃烧产生稳定的氧化物时所释放的热量。在25℃、101kPa,2mol S的燃烧放出的热量是1mol S的燃烧放出热量2倍,但是燃烧热是相同的。错误。C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH并不代表燃烧热。因为水在气态时是不稳定的状态,液态才是水的稳定状态。错误。D.在苯分子中不含C-C及C=C,而是存在一种介于单键与双键之间的一种特殊的化学键。因此根据表格提供的数据不能计算出该反应的反应热。正确。
考点:考查反应热、燃烧热、汽化热与化学键的关系的知识。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案下列过程需要吸收热量的是 ( )
①水蒸气冷凝②煅烧石灰石③浓硫酸稀释④酸碱发生中和反应⑤生石灰跟水反应生成熟石灰⑥干冰升华⑦液氨汽化⑧水分解为氢气和氧气⑨氢原子两两结合为氢分子
| A.①②⑤⑥⑨ | B.②③⑥⑨ | C.①④⑤⑦⑧ | D.②⑥⑦⑧ |
设NA代表阿伏伽德罗常数的值,则关于反应:C2H2 (g) + 5/2O2(g)=2CO2(g) + H2O(l) △H=-1300 kJ?mol-1的热化学方程式的说法中正确的是
| A.有10NA个电子转移时,该反应放出1300kJ的能量 |
| B.有NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.有2NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量 |
某学生实验小组用50 mL 0.50 mol·L-1的盐酸与50 mL 0.50 mol·L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定。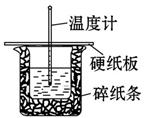
(1)图中装置缺少一种仪器,该仪器名称为______。
(2)下列说法正确的是______。
| A.小烧杯内残留有水,会使测得的反应热数值偏小 |
| B.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅 |
| C.烧杯间填满碎纸条的作用是固定小烧杯 |
| D.可用相同浓度和体积的硝酸代替稀盐酸溶液进行实验 |
用Cl2生产某些含氯有机物时会产生副产物HCl。 利用反应A:4HCl+O2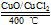 2Cl2+2H2O,
2Cl2+2H2O,
可实现氯的循环利用。
已知:Ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.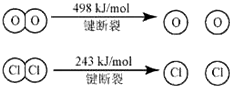
Ⅱ.则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
| A.16kJ | B.24kJ | C.32kJ | D.48kJ |
以下反应属于吸热反应的是:
| A.锌与稀硫酸的反应 | B.氯化铵与氢氧化钡晶体反应 |
| C.煤的燃烧 | D.氢氧化钠与盐酸的反应 |
下列热化学方程式正确的是( )
A.2SO2+O2 2SO3 ΔH=-196.6 kJ·mol-1 2SO3 ΔH=-196.6 kJ·mol-1 |
| B.C(g)+O2(g)=CO(g) ΔH=393.5 kJ·mol-1 |
C.H2(g)+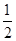 O2(g)=H2O(g) ΔH=-241.8 kJ O2(g)=H2O(g) ΔH=-241.8 kJ |
| D.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 |
化学与环境、能源、材料和科技等密切相关。下列说法中不正确的是( )
| A.鼓励汽车、家电“以旧换新”,可提高能源利用效率,与环境保护基本无关系 |
| B.农村大力发展沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.镁铝合金可用作制造飞机的材料 |
| D.氢氧燃料电池要广泛地应用于实际生产、生活中,高容量储氢材料的研制是需解决 |