题目内容
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol?L-1和1.5 mol?L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是
| A.反应后溶液中Fe3+物质的量为0.8 mol |
| B.反应后产生13.44 L H2(标准状况) |
| C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol |
| D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 |
C
试题分析:在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol?L-1和1.5 mol?L-1 n(Fe(NO3)3)=0.2mol;n(H2SO4)=1.5mol.n(Fe)=39.2g÷56g/mol=0.7mol.溶液中各离子的物质的量为n(Fe3+)= 0.2mol;n(NO3-)=0.6mol;n(H+)=3mol;n(SO42-)="1.5mol" .开始发生反应:Fe+4H++NO3-= Fe3++NO↑+ 2H2O.根据给定的微粒的物质的量的多少可知应该按照NO3-来进行计算。消耗Fe粉0.6mol,消耗H+2.4mol,还有剩余的氢离子0.6mol.产生NO气体0.6mol.这时溶液中含有Fe3+的物质的量为0.7mol.剩余铁粉发生反应:Fe+2Fe3+=3Fe2+.因为还含有铁粉0.1mol,Fe3+0.8mol根据二者关系可知铁粉完全反应产生0.3mol Fe2+还含有Fe3+0.6mol.因此在反应后的溶液中的Fe2+和Fe3+物质的量之和为0.9 mol 。A错误。C正确。 产生NO气体的物质的量为0.6mol.其在标准状况下体积为0.6mol×22.4l/mol="13.44L." B错误。在反应的过程中始终有气体产生,D错误。3)3和H2SO4的混合溶液中加入Fe粉发生的反应及前后顺序的知识。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
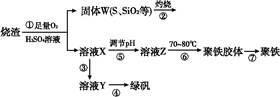
 2Cu + SO2
2Cu + SO2