题目内容
写出下列物质的电子式,有结构式的请写出结构式
①氨气 、 ②氯化铵 、
③干冰 、 ④苛性钠 、
⑤冰 、 ⑥过氧化钠 、
⑦双氧水 、 ⑧HClO 、
①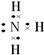
 ②
②
③ O=C=O ④
O=C=O ④
⑤ H—O—H ⑥
H—O—H ⑥
⑦ H—O—O—H ⑧
H—O—O—H ⑧ H—O—C
H—O—C
解析试题分析:书写化合物的电子式时应注意判断化合物的类型,属于离子化合物还是共价化合物。所给化合物中②④⑥属于离子化合物,其余是共价化合物。离子化合物的简单阳离子的电子式就是离子符号本身,阴离子及非简单阳离子的电子式需用[ ]表示,右上角注明离子所带电荷;共价化合物的电子式只表示共用电子对及不参与成键的最外层电子即可。离子化合物不存在结构式。详见答案。
考点:考查化合物的电子式、结构式的书写

如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
| 盐酸 分子式:HCl 相对分子质量:36.5,密度:1.19 g·cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为__ ____mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取___ _____mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面 ( )
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水 ( )
(4)①假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取________mL盐酸。(精确到小数点后一位)
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是________。
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
某厂平均每天产生约600 m3废氨水(NH3的浓度为153 mg·L-1,密度为1 g·cm—3。
(1)该废氨水中氨的物质的量浓度为 。
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3 的浓度降为17 mg·L-1。忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为 。(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO。4NH3+5O2 →4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80。
①为使NH3恰好完全氧化为NO,氨—空气混合物中氨的体积分数为________。
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2 →2N2+6H2O。将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1∶10,试求参加主反应的氨占原料氨的体积百分含量。
(4)废氨水可用于脱除烟气中的SO2。氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物。现称取不同质量的混合物进行实验,结果如下:
| NaOH 溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
试计算生成氨气的质量最大时样品的质量。
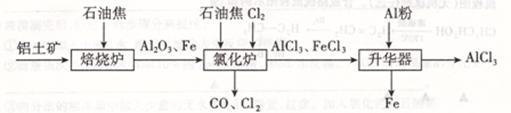
 2Fe(s) +3CO(g);
2Fe(s) +3CO(g); 2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,该样品中CaO2的物质的量为_____。
2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,该样品中CaO2的物质的量为_____。