题目内容
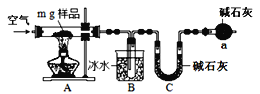
【题目】某研究小组利用如图装置探究SO2和Fe(NO3)3溶液的反应原理。下列说法错误的是( )
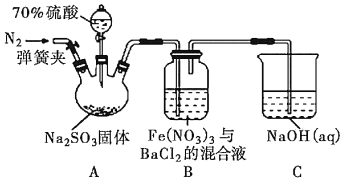
A.装置B中若产生白色沉淀,说明Fe3+能将SO2氧化成SO![]()
B.实验室中配制加70%的硫酸需要的玻璃仪器有量筒、烧杯、玻璃棒
C.三颈烧瓶中通入N2的操作应在滴加浓硫酸之前,目的是排尽装置内的空气
D.装置C可能发生倒吸,同时还不能完全吸收反应产生的尾气
【答案】A
【解析】
A. ![]() 具有氧化性,可将二氧化硫氧化成硫酸根,本身被还原成二价铁,反应的离子方程式是
具有氧化性,可将二氧化硫氧化成硫酸根,本身被还原成二价铁,反应的离子方程式是![]() ,在酸性条件下
,在酸性条件下![]() 与
与![]() 反应生成硫酸钡沉淀,出现白色沉淀,装置B中若产生白色沉淀,不能说明
反应生成硫酸钡沉淀,出现白色沉淀,装置B中若产生白色沉淀,不能说明![]() 能将
能将![]() 氧化成
氧化成![]() ,故A错误;
,故A错误;
B.配制![]() 硫酸溶液是浓硫酸加入水中稀释,需要的玻璃仪器有量筒、烧杯、玻璃棒,故B正确;
硫酸溶液是浓硫酸加入水中稀释,需要的玻璃仪器有量筒、烧杯、玻璃棒,故B正确;
C.为排除空气对实验的干扰,滴加浓硫酸之前应先通入氮气,目的是排尽装置内的空气,故C正确;
D.导气管直接插入溶液可能会引起装置中的压强变化较大发生倒吸,反应生成的气体可能会生成NO,不能被氢氧化钠溶液吸收,故D正确;
答案选A。

练习册系列答案
相关题目