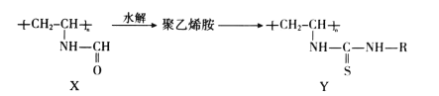
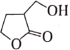
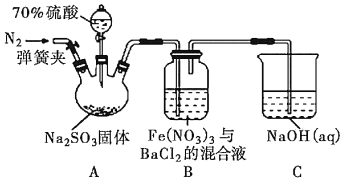
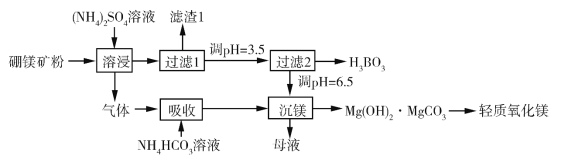
题目内容
【题目】常温下,向![]() 溶液中加入足量的镁条,该体系
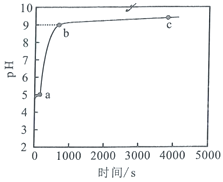
溶液中加入足量的镁条,该体系![]() 随时间变化的曲线如图所示。实验观察到
随时间变化的曲线如图所示。实验观察到![]() 点开始溶液中有白色沉淀生成,已知
点开始溶液中有白色沉淀生成,已知![]() 。下列说法错误的是( )
。下列说法错误的是( )
A.常温下,![]() 的水解平衡常数数量级为
的水解平衡常数数量级为![]()
B.体系中,水的电离程度大小关系为![]()
C.![]() 点时,溶液中
点时,溶液中![]()
D.![]() 点溶液中,
点溶液中,![]()
【答案】B
【解析】
A.常温下,氯化铵的水解平衡式为:NH4++H2ONH3H2O+H+,则Kh= ![]() ,由于氨水和氢离子浓度几乎相等,根据图像可知,没加镁之前,溶液的pH=5,c(NH3·H2O)≈c(H+)=10-5mol/L,c(NH4+)= 1mol/L,则Kh=
,由于氨水和氢离子浓度几乎相等,根据图像可知,没加镁之前,溶液的pH=5,c(NH3·H2O)≈c(H+)=10-5mol/L,c(NH4+)= 1mol/L,则Kh= ![]() =10-10,水解平衡常数数量级为
=10-10,水解平衡常数数量级为![]() ,故A正确;
,故A正确;
B.氯化铵的水解平衡式为:NH4++H2O NH3H2O +H+,加入镁单质时,消耗了氢离子,使平衡正向移动,促进铵根离子的水解,即促进了水的电离,故水的电离程度大小关系为c>b>a,故B错误;
C.![]() 点时,
点时,![]() ,pH=9,c(H+)=10-9mol/L,c(OH-)=10-5,c(Mg2+)=
,pH=9,c(H+)=10-9mol/L,c(OH-)=10-5,c(Mg2+)=![]() ,故C正确;
,故C正确;
D.![]() 点溶液中,电荷守恒式为:
点溶液中,电荷守恒式为:![]() ,故
,故
![]() ,故D正确;
,故D正确;
答案选B。

练习册系列答案
相关题目