题目内容
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-11。某溶液中含有Cl-,Br-,CrO42-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A. Cl-、Br-、CrO42- B. CrO42-、Br-、Cl-、
C. Br-、Cl-、CrO42- D. Br-、CrO42-、Cl-
【答案】C
【解析】
析出沉淀时,AgCl溶液中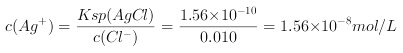 ;
;
AgBr溶液中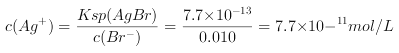 ;
;![]() 溶液中
溶液中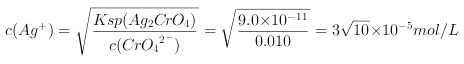 ,
,![]() 越小,则越先生成沉淀,所以种阴离子产生沉淀的先后顺序为:
越小,则越先生成沉淀,所以种阴离子产生沉淀的先后顺序为:![]() 、
、![]() 、
、![]() ,A. Cl-、Br-、CrO42-,故A错; B CrO42-、Br-、Cl-、故B错;C. Br-、Cl-、CrO42- ,故对;D Br-、CrO42-、Cl-故D错。
,A. Cl-、Br-、CrO42-,故A错; B CrO42-、Br-、Cl-、故B错;C. Br-、Cl-、CrO42- ,故对;D Br-、CrO42-、Cl-故D错。
因此,本题正确答案是:C。

练习册系列答案
相关题目