题目内容
【题目】向Fe 2 (SO 4 ) 3 和Al 2 (SO 4 ) 3 的混合溶液中,逐滴加入NaOH溶液至过量。下列图象中,能正确表示上述反应的是
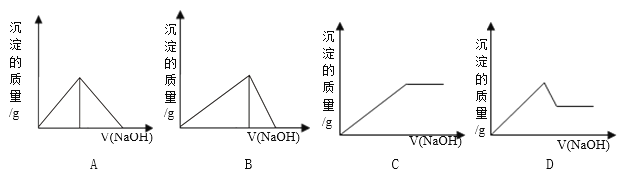
A. A B. B C. C D. D
【答案】D
【解析】因横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量,则向Fe 2 (SO 4 ) 3 和Al 2 (SO 4 ) 3 的混合溶液中,逐滴加入NaOH溶液,发生Fe 3++3OH-═Fe(OH)3↓、Al3++3OH-═Al(OH)3↓,则沉淀的质量一直在增大,直到最大;然后发生Al(OH)3+OH-═AlO2-+2H2O,沉淀的质量减少,但氢氧化铁不与碱反应,则最后沉淀的质量为一定值,显然只有D符合,故选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】除去下列物质中的杂质(括号内的物质),所使用的试剂和主要操作都正确的是
选项 | 物质 | 使用的试剂 | 主要操作 |
A | 乙醇(水) | 金属钠 | 蒸馏 |
B | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
C | 苯(苯酚) | 浓溴水 | 过滤 |
D | 乙烷(乙烯) | 溴水 | 洗气 |
A. A B. B C. C D. D