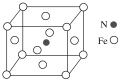
题目内容
【题目】有机物甲是芳香族化合物,取0.1mol有机物甲在足量氧气中完全燃烧后,生成0.7 mol CO2和5.4g H2O。甲的质谱如图所示,结构分析显示分子中存在 -OH和-COOH,苯环上有2种氢原子。
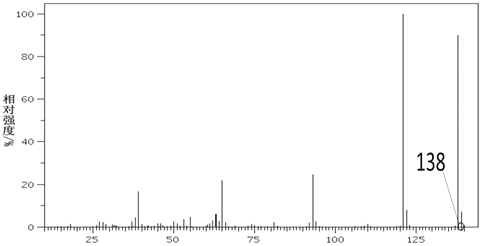
(1)甲的分子式为_______。
(2)甲的结构简式为____。
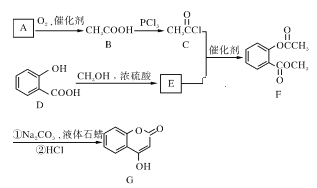
(3)甲可由相对分子量为92的芳香烃,经以下三步转化而得:
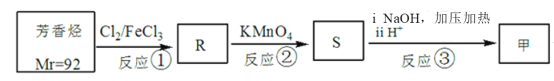
请写出S的结构简式____,以上流程中反应②和反应③能否互换___(填写“能”或者“不能”)。
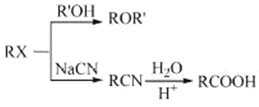
(4)已知:![]() CH3CH2CHO+
CH3CH2CHO+ 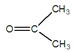 。某烃A的分子式为C6H10,经过上述转化生成
。某烃A的分子式为C6H10,经过上述转化生成![]() ,则烃A的结构可表示为:______。
,则烃A的结构可表示为:______。
【答案】C7H6O3 ![]()
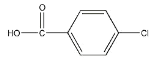 不能
不能 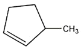
【解析】
0.1mol有机物甲在足量氧气中完全燃烧后,生成0.7 mol CO2和5.4g H2O,由此可知,1mol甲含有7mol C和6mol H,且从质谱图中看出甲的相对原子质量为138,可算出1mol甲中的氧原子数为:(138-7×12-6×1)/16= 3 mol,所以甲的分子式为:C7H6O3,根据结构分析显示分子中存在 -OH和-COOH,苯环上有2种氢原子,可写出甲的结构简式为:![]() 。由反应③的条件可知,反应③为碱性条件下的水解,然后进行酸化,由甲的结构简式即各反应的条件倒推出S、R、芳香烃的结构简式分别为:
。由反应③的条件可知,反应③为碱性条件下的水解,然后进行酸化,由甲的结构简式即各反应的条件倒推出S、R、芳香烃的结构简式分别为: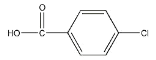 、
、 、
、 。
。
(1) 由分析可知甲的分子式为:C7H6O3;
(2) 根据分子式C7H6O3及结构分析显示分子中存在 -OH和-COOH,苯环上有2种氢原子,可写出甲的结构简式为:![]() ;
;
(3) S的结构简式为: ;若先进行反应③再进行反应②,则先转化为对甲基苯酚,但由于高锰酸钾具有强氧化性,所以能氧化苯酚,导致得不到甲这种产物,所以反应②和③的顺序不能互换;
;若先进行反应③再进行反应②,则先转化为对甲基苯酚,但由于高锰酸钾具有强氧化性,所以能氧化苯酚,导致得不到甲这种产物,所以反应②和③的顺序不能互换;
(4) 由已知:![]() CH3CH2CHO+
CH3CH2CHO+ 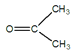 可发现,产物相当于由反应物断开反应物中的碳碳双键,双键两端产生C=O而得,根据产物的结构简式
可发现,产物相当于由反应物断开反应物中的碳碳双键,双键两端产生C=O而得,根据产物的结构简式 ![]() 及烃A的分子式为C6H10可推测出烃A的结构简式为:
及烃A的分子式为C6H10可推测出烃A的结构简式为: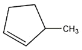 ,
, 在该条件下,双键被断开,引入C=O,因其C上含有H而构成醛基,产物为
在该条件下,双键被断开,引入C=O,因其C上含有H而构成醛基,产物为![]() ,验证所推测的A的结构简式是正确的。
,验证所推测的A的结构简式是正确的。

【题目】下列实验能达到实验目的的是( )
实验目的 | 实验操作 | |
A | 比较S和Si的非金属性强弱 | 向Na2SiO3溶液中通入SO2产生白色沉淀 |
B | 除去NaHCO3溶液中的杂质Na2CO3 | 向混合液中通入足量的CO2气体 |
C | 检验某盐是否为铵盐 | 试样 |
D | 验证H2O2和Fe3+的氧化性 强弱 | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
A. A B. B C. C D. D