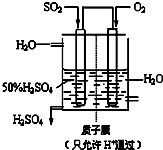
题目内容
含有硫的化合物在工业生产中应用广泛,回答下列问题:
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2。
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数。
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取
研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100 mL滴有淀粉的
蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体
积为20.00mL。求该黄铜矿的纯度。
(2)将FeS和Fe2O3的混和物56.6 g,用足量稀H2SO4溶解后可得3.2 g硫,原混和物中FeS的质量。
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧
化钠溶液吸收。利用下图装置加热无水硫酸铜粉末直至完全分解。若无水硫酸铜粉末质量为10.0 g,
完全分解后,各装置的质量变化关系如下表所示。
|
装置 |
A(试管+粉末) |
B |
C |
|
反应前 |
42.0 g |
75.0 g |
140.0 g |
|
反应后 |
37.0 g |
79.0 g |
140.5 g |

请通过计算,推断出该实验条件下硫酸铜分解的化学方程式。
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4
+ 4C Na2S + 4CO↑ ②Na2SO4
+ 4CO
Na2S + 4CO↑ ②Na2SO4
+ 4CO Na2S + 4CO2
Na2S + 4CO2
a.若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量。
b.硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量。
(1) ① 20% ②80% (各2分,共4分)
(2) 8.8 g ;40.6 g (各2分,共4分)
(3)4CuSO4 4CuO + 2SO3↑+ 2SO2↑+
O2↑ (2分)
4CuO + 2SO3↑+ 2SO2↑+
O2↑ (2分)
(4) a.0.5 < n(Na2S)<1 (2分)
b.n(Na2S)=0.15 mol ;n(Na2SO3)=0.05 mol ;n(Na2SO4)=0.01 mol
n(H2O)=1.35 mol (合理即给分。各1分,共4分)
【解析】
试题分析:(1)①根据化学式CuFeS2可知,该化合物中铜和硫的质量之比是64:64=1:1,所以该矿石含铜的质量分数等于硫的质量分数,都是20%。
②消耗单质碘的物质的量是0.05mol/L×0.020mol/L=0.0010mol,则根据方程式I2+SO2+2H2O=H2SO4+2HI可知,10ml溶液中含有SO2的物质的量是0.010mol,所以生成的SO2的物质的量是0.0010mol× =0.0100mol,所以根据硫原子守恒可知,CuFeS2的物质的量是0.0100mol÷2=0.0050mol,其质量=0.0050mol×184g/mol=0.82g,所以该黄铜矿的纯度
=0.0100mol,所以根据硫原子守恒可知,CuFeS2的物质的量是0.0100mol÷2=0.0050mol,其质量=0.0050mol×184g/mol=0.82g,所以该黄铜矿的纯度 ×80%=80%。
×80%=80%。
(2)生成单质S的物质的量是3.2g÷32g/mol=0.1mol。反应中如果铁离子不足,则根据关系式2Fe3+~S可知,铁离子的物质的量是0.2mol,因此氧化铁的物质的量是0.1mol,其中质量是160g/mol×0.1mol=16g,因此FeS的质量是56.6g-16g=40.6g;如果反应中铁离子过量,则根据硫原子守恒可知,FeS的物质的量是0.1mol,质量是0.1mol×88g/mol=8.8g。
(3)硫酸铜的物质的量=10.0g÷160g/mol=0.0625mol。试管A的质量是42.0g-10.0g=32.0g,所以反应后生成的氧化铜的质量是37.0g-32.0g=5.0g,物质的量是5.0g÷80g/mol=0.0625mol。则生成物SO2、三氧化硫和氧气质量之和是10.0g-5.0g=5.0g。B和C装置是吸收SO2和三氧化硫的,因此二者的质量之和是4.5g,所以氧气的质量是5.0g-4.5g=0.5g,其物质的量是0.5g÷32g/mol= 0.015625mol。设SO2和三氧化硫的物质的量分别是x和y,则x+y=0.0625mol、64x+80y=4.5g,解得x=y=0.03125mol,所以氧化铜、SO2、三氧化硫和氧气的物质的量之比是4:2:2:1,因此该反应的化学方程式是4CuSO4 4CuO + 2SO3↑+ 2SO2↑+
O2↑。
4CuO + 2SO3↑+ 2SO2↑+
O2↑。
(4)a.若反应中生成的气体只有CO,则根据反应①可知,生成的硫化钠物质的量=2mol÷4=0.5mol;若反应中生成的气体只有CO2,则根据反应①②可知Na2SO4 + 2C Na2S + 2CO2↑,所以生成的硫化钠物质的量=2mol÷2=1mol,因此硫化钠的物质的量是0.5 < n(Na2S)<1。
Na2S + 2CO2↑,所以生成的硫化钠物质的量=2mol÷2=1mol,因此硫化钠的物质的量是0.5 < n(Na2S)<1。
b.在滤液中加入足量的BaCl2后过滤得2.33g沉淀,该白色沉淀是硫酸钡,其物质的量是2.33g÷233g/mol=0.01mol,因此根据原子守恒可知,硫酸钠的物质的量是0.01mol。4.8g沉淀是S,其物质的量是4.8g÷32g/mol=0.15mol,则根据方程式2Na2S+Na2SO3+6HCl=6NaCl+3S↓+3H2O可知,硫化钠和亚硫酸钠的物质的量分别是0.10mol和0.05mol。1.12L H2S 气体的物质的量=1.12L÷22.4L/mol=0.05mol,所以根据方程式Na2S+2HCl=6NaCl+H2S↑可知,硫化钠的物质的量=0.05mol,因此硫化钠的物质的量共计=0.15mol。因此结晶水的质量=43.72g-0.15mol×78g/mol-0.05mol×126g/mol-0.01mol×142g/mol=24.3g,所以结晶水的物质的量=24.3g÷18g/mol=1.35mol。
考点:考查元素含量、物质纯度、物质成分的有关计算以及方程式的书写等

 含有硫的化合物在工业生产中应用广泛,回答下列问题:
含有硫的化合物在工业生产中应用广泛,回答下列问题:
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2.
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数.
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100mL滴有淀粉的蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体积为20.00mL.求该黄铜矿的纯度.
(2)将FeS和Fe2O3的混和物56.6g,用足量稀H2SO4溶解后可得3.2g硫,求原混和物中FeS的质量.
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2.已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收.利用下图装置加热无水硫酸铜粉末直至完全分解.若无水硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示.
| 装置 | A (试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4+4C
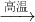 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO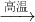 Na2S+4CO2
Na2S+4CO2①若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量.
②硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量.
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2.
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数.
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100mL滴有淀粉的蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体积为20.00mL.求该黄铜矿的纯度.
(2)将FeS和Fe2O3的混和物56.6g,用足量稀H2SO4溶解后可得3.2g硫,求原混和物中FeS的质量.
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2.已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收.利用下图装置加热无水硫酸铜粉末直至完全分解.若无水硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示.
| 装置 | A (试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4+4C
 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO Na2S+4CO2
Na2S+4CO2①若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量.
②硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量.

 (2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:
(2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题: