题目内容
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。葡萄糖酸亚铁的制备方法之一是由新制备的碳酸亚铁(白色固体,微溶于水)与葡萄糖酸反应而制得,其流程如下:
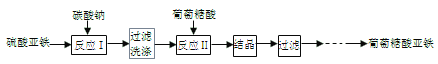
(1)用下图装置制备FeCO3
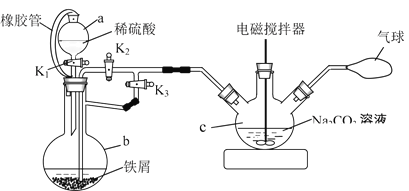
①仪器b的名称为_________。仪器a中橡胶管的作用是_______。
②反应开始时,先打开活塞K1和K3,关闭K2,目的是_______。一段时间后,关闭_______,打开______,目的是_______。
③将制得的FeCO3过滤、洗涤。检验沉淀已经洗涤干净的试剂为______(若多种试剂,按试剂使用由先到后的顺序填写)。
④用NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,反应的离子方程式为________。
(2)反应II中加入过量葡萄糖酸使溶液显弱酸性,原因是________。
(3)葡萄糖酸亚铁结晶时需加入乙醇,目的是____________。
【答案】蒸馏烧瓶 使内外压强相通,液体能顺利流下 排出装置中的空气 K3 K2 将b中溶液压入装置c中 盐酸 、 BaCl2溶液或Ba(NO3)2溶液 Fe2++2HCO3-=FeCO3↓+H2O+CO2↑ 防止Fe2+水解生成Fe(OH)2 降低葡萄糖酸亚铁在水中溶解度,便于葡萄糖酸亚铁结晶析出
【解析】
亚铁离子容易被氧气氧化,制备过程中应在无氧环境中进行,Fe与稀硫酸反应制备硫酸亚铁,利用反应生成的氢气排尽装置中的空气,故烧瓶b中制备硫酸亚铁,三颈烧瓶c中FeSO4和Na2CO3发生反应:FeSO4+Na2CO3=FeCO3↓+Na2SO4,利用生成氢气,使烧瓶中气压增大,将硫酸亚铁溶液压入三颈烧瓶中,据此分析解答。
(1)①根据仪器b的构造名称为蒸馏烧瓶;实验过程中要保证分液漏斗中的液体顺利流下,仪器a中橡胶管的作用是使内外压强相通,液体能顺利流下;
②亚铁离子容易被氧气氧化,制备过程中应在无氧环境中进行,Fe与稀硫酸反应制备硫酸亚铁,利用反应生成的氢气排尽装置中的空气;一段时间后,关闭K3,打开K2,利用生成氢气,使烧瓶中气压增大,将b中硫酸亚铁溶液压入装置c中;
③将根据信息可知,亚铁离子容易被氧气氧化,所以将制得的碳酸亚铁浊液过滤、洗涤。检验FeCO3已经洗涤干净即确定其表面是否有附着的硫酸钠,即检验硫酸根离子,去最后一次洗涤液,先用盐酸酸化排除干扰,再加入BaCl2溶液或Ba(NO3)2溶液,若产生白色沉淀说明FeCO3未洗涤干净,若溶液澄清无沉淀生成,则说明FeCO3已经洗涤干净;
④C中反应方程式是FeSO4+Na2CO3=FeCO3↓+Na2SO4,若用NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时生成二氧化碳,反应的离子方程式为Fe2++2HCO3-=FeCO3↓+H2O+CO2↑;
(2)根据信息可知,亚铁离子容易被氧气氧化,也易水解成氢氧化亚铁沉淀,所以反应Ⅱ后加入葡萄糖酸调节溶液pH至5.8,其原因是防止Fe2+水解生成Fe(OH)2沉淀;
(3)根据信息可知:葡萄糖酸亚铁易溶于水,几乎不溶于乙醇,所以葡萄糖酸亚铁溶液结晶、洗涤时均需加入乙醇,其目的都是降低葡萄糖酸亚铁在水中溶解度,便于葡萄糖酸亚铁结晶析出。

【题目】[实验化学]
3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33 ~36 |
| 易溶于甲醇、乙醚,微溶于水 |
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取。①分离出甲醇的操作是的_________。
②萃取用到的分液漏斗使用前需_______并洗净,分液时有机层在分液漏斗的_____填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3溶液洗涤的目的是______________;用饱和食盐水洗涤的目的是______________。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是_____(填字母)。
a.蒸馏除去乙醚 b..重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤。为了防止倒吸,减压过滤完成后应先_______,再______。