题目内容
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率;
B. 合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率;
C. 在实验室里,可用碳酸钙粉末和稀硫酸制得二氧化碳气体;
D. 实验室用排饱和食盐水的方法收集氯气。
【答案】C
【解析】试题分析:A、在二氧化硫的催化氧化反应中,通入过量的空气以提高二氧化硫的转化率,增大氧气浓度平衡正向进行,和平衡有关,可以勒夏特列原理解释,故A能;B、合成氨的反应为气体体积缩小的反应,则采用20MPa~50MPa压强,有利于平衡正向移动,以提高原料的利用率,能解释,故B能;C、碳酸钙粉末和稀盐酸制得二氧化碳气体的反应,增大固体的表面积,反应速率加快,与化学平衡无关,不能用勒夏特列原理解释,故C不能;D、氯化钠在溶液中完全电离,所以饱和食盐水中含有大量的氯离子,氯气溶于水的反应是一个可逆反应,Cl2+H2O![]() ClO-+2H++Cl-,由于饱和食盐水中含有大量的氯离子,相当于氯气溶于水的反应中增加了大量的生成物氯离子,根据勒夏特列原理,平衡向逆反应方向移动,氯气溶解量减小,所以可以勒夏特列原理解释,故D能;故选C。
ClO-+2H++Cl-,由于饱和食盐水中含有大量的氯离子,相当于氯气溶于水的反应中增加了大量的生成物氯离子,根据勒夏特列原理,平衡向逆反应方向移动,氯气溶解量减小,所以可以勒夏特列原理解释,故D能;故选C。

 名校课堂系列答案
名校课堂系列答案【题目】某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)
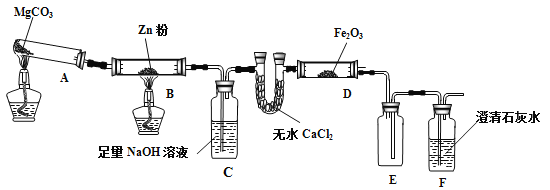
(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。(Fe2+ 遇K3[Fe(CN)6]溶液会生成蓝色沉淀)
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是 。
②甲组步骤1中反应的离子方程式为 。
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因为 。
④从实验安全考虑,题图装置还可采取的改进措施是 。
