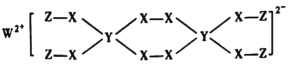题目内容
【题目】在标准状况下,由一氧化碳和二氧化碳组成的混合气体为6.72 L,质量为12g,此混合物中一氧化碳和二氧化碳物质的量之比是__________,一氧化碳的体积分数是__________,一氧化碳的质量分数是__________,碳原子和氧原子个数比是__________,混合气体的平均相对分子质量是__________,密度是__________g·L-1。
【答案】1∶3 25% 17.5% 4∶7 40 1.79
【解析】
根据公式:![]() =
=![]() 进行分析解答。
进行分析解答。
混合气体的物质的量=![]() =0.3 mol,
=0.3 mol,
设一氧化碳的物质的量为x,二氧化碳的物质的量为y,则:
![]()
解得:x=0.075 mol,y=0.225 mol,
此混合物中一氧化碳和二氧化碳物质的量之比=0.075mol∶0.225 mol=1∶3;
一氧化碳的体积分数是=![]() ×100% =25% ;
×100% =25% ;
一氧化碳的质量=0.075 mol×28g·mol-1=2.1 g,
一氧化碳的质量分数=![]() ×100% =17.5% ;
×100% =17.5% ;
碳原子和氧原子个数比=(0.075 mol+0.225 mol)∶(0.075 mol+0.225mol×2)=4∶7;
混合气体的平均摩尔质量=![]() =40g·mol-1,平均相对分子质量是40;
=40g·mol-1,平均相对分子质量是40;
混合气体的密度=![]() ≈1.79 g·L-1。答案:1∶3;25% ;17.5% ;4∶7; 40;1.79。
≈1.79 g·L-1。答案:1∶3;25% ;17.5% ;4∶7; 40;1.79。

【题目】某化学研究性学习小组的同学根据理论分析后认为,NO2可能会氧化单质铜,他们设想利用下图所示装置验证NO2的氧化性(夹持装置已省略)。
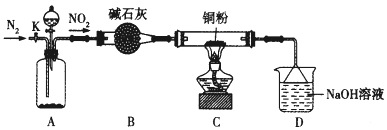
(1)装置A~C中有一处错误,改正的方法是_____________,A中发生反应的两种试剂通常是________。
(2)点燃C处酒精灯比较合适的时机是_____________。若C中固体全部变成黑色,同时生成对环境无污染的气体,写出C中反应的化学方程式:______________。装置D的用途是____________。
(3)开关K的设计是以实现绿色化学实验为目的,请说明K的使用方法______________。(包括使用时段与内容)。
(4)实验结束后发现C中的固体混有少量的红色粉末,经过分析,甲同学认为该红色粉末是Cu2O,乙同学认为该红色粉末是![]() ,丙同学认为该红色粉末是Cu和Cu2O的混合物。查阅资料,Cu、Cu2O和CuO的部分性质如下:
,丙同学认为该红色粉末是Cu和Cu2O的混合物。查阅资料,Cu、Cu2O和CuO的部分性质如下:
稀硫酸 | 氨水 | |
Cu2O | 生成Cu和Cu2+ | 生成无色[Cu(NH3)2]2+ |
CuO | 生成Cu2+ | 生成蓝色[Cu(NH3)4]2+ |
Cu | --- | --- |
请设计一个简单的实验证明甲同学的看法是否正确:________________。