题目内容
13.下列表示正确的是( )| A. | CO2的电子式: | B. | 乙烯的结构式:CH2═CH2 | ||
| C. | CH4的比例模型: | D. | Cl-离子的结构示意图: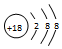 |
分析 A、CO2是共价化合物,其结构式为O=C=O;
B、乙烯的结构式中C-H不能省略;
C、甲烷为正面体结构,由原子相对大小表示空间结构为比例模型;
D、氯离子的核内有17个质子.
解答 解:A、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故A错误;
,故A错误;
B、乙烯的结构式中C-H不能省略,乙烯的结构式为: ,故B错误;
,故B错误;
C、甲烷为正面体结构,由原子相对大小表示空间结构为比例模型,则CH4分子的比例模型为 ,故C正确;
,故C正确;
D、氯离子的核内有17个质子,核外有18个电子,故结构示意图为 ,故D错误.
,故D错误.
故选C.
点评 本题考查了常见的化学用语,难度不大,应注意的是原子结构示意图和离子结构示意图的区别.

练习册系列答案
相关题目
3.现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍.下列说法正确的是( )
| A. | 简单阳离子的氧化性:Y>X | |
| B. | 气态氢化物的沸点:Z>M | |
| C. | X、Z与M不可能存在同一离子化合物中 | |
| D. | Y2Z的溶液:c(Y+):c(Z2-)>2:1 |
4.将足量CO2气体通入水玻璃(Na2SiO3溶液)中,然后加热蒸干,再在高温下充分灼烧,最后所得的固体物质是( )
| A. | Na2CO3、Na2SiO3 | B. | Na2CO3、SiO2 | C. | Na2SiO3 | D. | SiO2 |
1.下列离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O=2H++C1-+C1O- | |
| B. | 硫酸铝溶液中加入足量氨水:Al3++4OH-=AlO2-+2H2O | |
| C. | FeS04溶液与稀硝酸反应:3Fe2++NO3-+4H+=3Fe3++NO+2H2O | |
| D. | 稀硫酸中加入铁粉:2Fe+6H+═2Fe3++3H2↑ |
18.下列说法正确的是( )
| A. | Mg3N2晶体中的化学键是共价键 | |
| B. | 某物质含有离子键,则该物质在任何条件下均能导电 | |
| C. | 干冰是分子晶体,其气化过程中只需克服分子间作用力 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
5.在c(Na+)为0.5mol•L-1的某溶液中,还可能含有下表中的若干离子.
取该溶液100mL进行如下实验(不考虑气体的溶解且气体体积是在标准状况下测定的).
试回答下列问题.
(1)由实验Ⅰ、Ⅱ可以得出的结论是原溶液中一定存在的离子有NH4+、CO32-、SO42-.
(2)实验Ⅱ中沉淀被溶解的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,Mg2+与CO32-不能大量共存的原因是Mg2++CO32-=MgCO3↓(用离子方程式表示).
(3)由实验Ⅲ得出原溶液中含有Cl-,你认为该观点是否正确?不正确(填“正确”或“不正确”),原因是步骤Ⅱ加入了氯离子.
(4)填写下表中各离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“×”)
(5)你认为原溶液中是否存在NO3-?不能确定(填“存在”、“不存在”或“不能确定”).原溶液中同时存在Cl-和NO3-,则c(NO3-)+c(Cl-)=0.4mol•L-1.
| 阳离子 | NH4+、Mg2+ |
| 阴离子 | Cl-、CO32-、SO42-、NO3- |
| 序号 | 实验内容 | 实验现象 |
| Ⅰ | 向该溶液中加入足量Ba(OH)2溶液并加热 | 产生6.27g白色沉淀并放出1.12L有刺激性气味的气体 |
| Ⅱ | 将Ⅰ得到的沉淀中滴加足量的稀盐酸 | 有气体放出,沉淀变为2.33g |
| Ⅲ | 向Ⅱ反应后的滤液中滴加AgNO3溶液 | 有白色沉淀产生 |
(1)由实验Ⅰ、Ⅱ可以得出的结论是原溶液中一定存在的离子有NH4+、CO32-、SO42-.
(2)实验Ⅱ中沉淀被溶解的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,Mg2+与CO32-不能大量共存的原因是Mg2++CO32-=MgCO3↓(用离子方程式表示).
(3)由实验Ⅲ得出原溶液中含有Cl-,你认为该观点是否正确?不正确(填“正确”或“不正确”),原因是步骤Ⅱ加入了氯离子.
(4)填写下表中各离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“×”)
| 阴离子 | NH4+ | Mg2+ | CO32- | SO42- |
| c/mol•L-1 | 0.5mol/L | × | 0.2mol/L | 0.1mol/L |
2.关于硫及其化合物说法正确的是( )
| A. | 自然界的硫元素主要以硫单质、硫化物和硫酸盐等形式存在 | |
| B. | 浓硫酸可作干燥剂,但不能干燥二氧化硫、氯气等气体 | |
| C. | 二氧化硫能使溴水褪色,说明其具有漂白性 | |
| D. | 浓硫酸中存在的主要是硫酸分子,常温下就能和铜片剧烈反应 |
8.一种熔融碳酸盐燃料电池的工作原理如图.下列有关该电池的说法不正确的是( )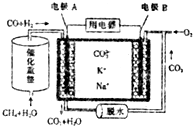

| A. | 电流方向:由B极经用电器流向A极 | |
| B. | 电极B上发生的电极反应为2CO2+O2+4e-═CO22- | |
| C. | 电池工作时,K+、Na+向电极B移动 | |
| D. | 若消耗电极B上的O233.6L(标准状况),则至少需要1moL CH4参加反应 |