题目内容
12.用NA表示阿伏加德罗常数,下列有关说法正确的是( )| A. | 在常温常压下,11.2LO2含有的分子数为0.5NA | |
| B. | 在常温常压下,1mol氦气含有的原子数为2NA | |
| C. | 71gCl2所含原子数为2NA | |
| D. | 标准状况下,1molH2O和1 molH2的体积都约为22.4L |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、氦气为单原子分子;
C、求出氯气的物质的量,然后根据氯气为双原子分子来分析;
D、标况下水为液态.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氧气的物质的量小于0.5mol,则分子数小于0.5NA个,故A错误;
B、氦气为单原子分子,故1mol氦气中含1mol氦原子即NA个,故B错误;
C、71g氯气的物质的量为1mol,而氯气为双原子分子,故1mol氯气中含2mol原子即2NA个,故C正确;
D、标况下水为液态,故1mol水的体积小于22.4L,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
3.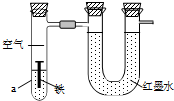 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )| A. | 铁钉表面发生的反应为Fe-3e-=Fe3+ | |
| B. | 若液体a为稀盐酸,则U形管液面右高左低 | |
| C. | 若液体a为食盐水,则U形管液面左高右低 | |
| D. | 若液体a为食用油,则铁钉生锈速率较慢 |
20.下列制取蒸馏水的实验装置与操作的说法中,不正确的是( )
| A. | 可用过滤的方法制取蒸馏水 | |
| B. | 冷凝器中的水流方向是从下口进入,上口排出 | |
| C. | 实验中需要在蒸馏烧瓶中加入几片碎瓷片或沸石 | |
| D. | 给蒸馏烧瓶加热时要垫上石棉网 |
7.下列实验事实陈述正确并且有因果关系的是( )
| A. | 滴加BaC12溶液生成白色沉淀 原溶液中有SO42- | |
| B. | 用洁净铂丝蘸取溶液进行焰色反应:火焰呈黄色 原溶液中有Na+无K+ | |
| C. | 滴加氯水和CC14,振荡、静置.下层溶液显紫色 原溶液中有I- | |
| D. | 滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝 原溶液中无NH4+ |
17.下列描述正确的是( )
| A. | 氯水的标签上应标注: | B. | O2-的结构示意图: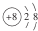 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | BeCl2的电子式: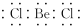 |
2.可用电解法将粗铜变为精铜,粗铜中所含杂质为Fe、Ni、Ag和Au,用硫酸铜溶液作电解液.已知,氧化性:Cu2+>Ni2+>Fe2+.则以下叙述错误的是( )
| A. | 粗铜在阳极的反应顺序是:Fe-2e-═Fe2+、Ni-2e-═Ni2+、Cu-2e-═Cu2+,杂质金和银不反应形成“阳极泥” | |
| B. | 电解一段时间后,溶液中Cu2+减小 | |
| C. | 若电路中通过1 mol电子,阳极有0.5 mol铜被氧化 | |
| D. | 阴极反应只有Cu2++2e-═Cu |
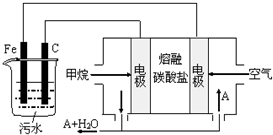 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污 物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污 物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.