题目内容
已知:N2(g)+3H2(g) ===2NH3(g) ΔH=-92.4 kJ·mol-1
下列说法正确的是
A.反应中的能量变化如图所示,则ΔH=E1-E3
B.若加入催化剂,将改变反应历程,从而改变ΔH
C.温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1
D.若保持温度和容器体积不变,充入氦气,则压强增大,化学反应速率加快

C

练习册系列答案
相关题目


 2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。
2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。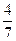 。计算该条件下达到平衡时N2转化率为 ;
。计算该条件下达到平衡时N2转化率为 ;