题目内容
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
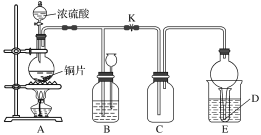
实验中某同学将a g铜片和12 mL 18 mol·L-1的浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。
请回答:
(1)请写出Cu与浓硫酸反应的化学方程式:_____________________________。
(2)装置E中试管D内盛品红溶液,当C中气体收集满后,D中有可能观察到的现象是______________________。
实验装置E中D有可能造成环境污染,试用最简单方法加以解决(实验用品自选)______________。
装置B的作用是储存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是____________________。B中应放置的液体是________(填字母)。
A 饱和Na2SO3溶液 B 酸性KMnO4溶液 C 浓溴水 D 饱和NaHSO3溶液
(3)问题讨论:为什么有一定量的余酸还未能使Cu完全溶解。你认为原因是______________________。
足量下列药品能够用来证明反应结束后的烧瓶中的确有余酸的是________(填字母)。
A Fe B BaCl2溶液 C Ag D Na2CO3溶液
(4)实验中该同学向A中反应后溶液中通入一种气体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是__________(填名称),反应的化学方程式是__________________________________。
【答案】Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O 品红溶液褪色 用浸有NaOH溶液的棉花团塞在试管口 广口瓶中液面下降,长颈漏斗中液面上升 D 随着H2SO4的消耗,浓H2SO4浓度逐渐变稀,稀硫酸与铜不反应 AD 氧气 2Cu+2H2SO4+O2
CuSO4+SO2↑+2H2O 品红溶液褪色 用浸有NaOH溶液的棉花团塞在试管口 广口瓶中液面下降,长颈漏斗中液面上升 D 随着H2SO4的消耗,浓H2SO4浓度逐渐变稀,稀硫酸与铜不反应 AD 氧气 2Cu+2H2SO4+O2![]() 2CuSO4+2H2O
2CuSO4+2H2O
【解析】
(1)Cu与浓H2SO4反应需加热;
(2)SO2能使品红溶液褪色,为防止环境污染,可用的简单方法是用浸有NaOH溶液的棉花团塞在试管口;
A、Na2SO3+H2O+SO2=2NaHSO3;
B、KMnO4氧化SO2;
C、Br2+SO2+2H2O===2HBr+H2SO4;
D、SO2难溶于饱和NaHSO3溶液;
(3)随着反应的进行浓H2SO4浓度降低,变为稀H2SO4,Cu与稀H2SO4不反应;
(4)根据题目要求气体单质应为强氧化剂,且仅生成CuSO4溶液,该氧化剂为O2。
(1)Cu与浓H2SO4反应需加热,反应生成硫酸铜、二氧化硫和水,反应的化学方程式为Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)SO2能使品红溶液褪色,为防止环境污染,可用的简单方法是用浸有NaOH溶液的棉花团塞在试管口,即SO2+2NaOH=Na2SO3+H2O。关闭K装置内气体压强增大,B广口瓶内液面下降,长颈漏斗内液面上升;B中的液体应不能与SO2反应,而且要防止SO2的溶解;
A、亚硫酸钠溶液能吸收SO2,发生的反应为Na2SO3+H2O+SO2=2NaHSO3;
B、KMnO4氧化SO2;
C、溴水能吸收SO2,发生的反应为Br2+SO2+2H2O=2HBr+H2SO4;
D、SO2难溶于饱和NaHSO3溶液。
答案选D;
(3)随着反应的进行浓H2SO4浓度降低,变为稀H2SO4,Cu与稀H2SO4不反应。检验余酸实质是检验H+的存在。Fe+2H+=Fe2++H2↑(现象为产生大量气泡),CO32-+2H+=H2O+CO2↑(现象为产生大量气泡),Fe和Na2CO3溶液能证明H+的存在;BaCl2溶液不能证明H2SO4剩余,因为产物CuSO4也能电离出SO42-;Ag与H+不反应,不能证明H+的存在。
答案选AD;
(4)根据题目要求气体单质应为强氧化剂,且仅生成CuSO4溶液,该氧化剂为O2,反应的化学方程式为2Cu+2H2SO4+O2![]() 2CuSO4+2H2O。
2CuSO4+2H2O。

【题目】2014年,全国很多地区都曾出现严重的雾霾天气,汽车尾气、冬季取暖排放的CO2等都是形成雾霾的因素。请回答下列问题:
将不同物质的量的H2O(g)和CO分别通入容积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g)![]() CO2(g)+H2(g),得到3组数据如表所示:
CO2(g)+H2(g),得到3组数据如表所示:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡状态所需时间/min | ||
H2O | CO | CO | H2 | |||
1 | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
2 | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
3 | 900 | a | b | c | d | t |
(1)实验1中0~5min内,以v(CO2)表示的化学反应速率为______,此温度下的化学平衡常数为______,温度升高时化学平衡常数会_______(填“增大”“减小”或“不变”)。
(2)若a=2,b=1,则达到平衡状态时实验2中H
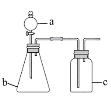
【题目】用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到实验目的的是
选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 | 装置 |
A | 氨水 | CaO | 无 | 制取并收集氨气 |
|
B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 制备纯净的Cl2 | |
C | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 比较酸性强弱: H2CO3>H2SiO3 | |
D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | 验证SO2具有还原性 |
A.AB.BC.CD.D