题目内容
As2S3和HNO3有如下反应:As2S3+10HNO3 2H3AsO4+3S+10NO2+2H2O,下列说法正确的是
| A.该反应的氧化产物仅为S |
| B.生成1molH3AsO2时。转移电子个数为10NA |
| C.将反应设计成一原电池,则NO2应该在正极附近逸出 |
| D.反应产生的NO2与56LO2混合在水中正好完全反应生成硝酸 |
C
解析试题分析:A、标出反应物和生成物中各元素的化合价,As、S的化合价升高,发生了氧化反应,故氧化产物有两种,错误;B、由方程式可知,生成2molH2AsO4的同时生成10molNO2,转移电子数为10NA,错误;C、原电池中正极发生还原反应生成还原产物,正确;D、在NO2的量未知的前提下无法确定消耗O2的量,错误。
考点:考查氧化还原反应,考查考生综合应用氧化还原原理处理问题的能力。

同位素示踪法可用于反应机理的研究,下列反应中,同位素示踪表示正确的是
| A.CH3COOH+C2H18 5OH→CH3COOC2H5+H18 2O |
B.NH4Cl+2H2O NH3·2H2O+HCl NH3·2H2O+HCl |
| C.K37ClO3+6HCl=K37Cl+3Cl2↑+3 H2O |
| D.2KMnO4+5H218O2+3H2SO4=K2SO4+2MnSO4+518O2↑+8H2O |
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列不正确的是( )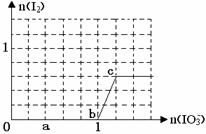
| A.0~b :3HSO3-+ IO3-= 3SO42-+ I-+ 3H+ |
| B.a点时消耗NaHSO3的物质的量为1.2 mol |
| C.b~c间I2是还原产物 |
| D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3为1.8mol |
常温下,在下列溶液中发生如下反应
①16H++10Z-+2XO4-→2X2++5Z2+8H2O ②2A2+ +B2→2A3++2B-
③2B-+Z2→B2+2Z-
由此判断下列说法错误的是( )
| A.反应Z2+2A2+=2A3++2Z-可以进行。 |
| B.还原性由强到弱的顺序是A2+、B-、Z-、X2+ |
| C.氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ |
| D.Z元素在①③反应中均被还原 |
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O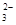 +O2+xOH—
+O2+xOH— Fe3O4+S4O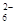 +2H2O,
+2H2O,
下列说法中,正确的是( )
| A.每生成1mol Fe3O4,反应转移的电子总数为3mol ; |
| B.x="6" |
| C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol; |
| D.Fe2+和S2O32—-都是还原剂; |
氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得: SiO2 + C + N2 Si3N4 + CO
Si3N4 + CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是 。
(3)分析反应可推测碳、氮气的氧化性:C N2(填“>”“<”“=”)。
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是 。
| A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
| B.在电子工业上制成耐高温的电的良导体 |
| C.研发氮化硅的全陶发动机替代同类型金属发动机 |
| D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
已知2Al+2NaOH+2H2O 2NaAlO2+3H2。该反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
2NaAlO2+3H2。该反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
| A.每生成0.3 mol H2,被还原的水分子数目为0.6 NA |
| B.当有2.7 g Al参加反应时,转移的电子数目为0.3 NA |
| C.每生成6.72 L的H2,溶液中AlO2-的数目就增加0.2 NA |
| D.溶液中每增加0.1 mol的AlO2-,Na+的数目就增加0.1 NA |
在化学分析实验中,常常用到酸碱滴定、沉淀滴定、氧化还原滴定等。下列属于氧化还原滴定的是
| A.用标准盐酸滴定NaOH溶液 |
| B.用标准KMnO4溶液滴定FeSO4溶液 |
| C.用标准KSCN溶液滴定FeCl3溶液 |
| D.用标准AgNO3溶液滴定NaCl溶液 |
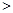 NaNO2 B.氧化性:NaNO2
NaNO2 B.氧化性:NaNO2