题目内容
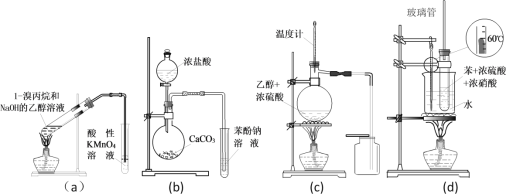
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,如图1装置(铁架台、酒精灯等略)验证取代反应和消去反应的产物,请你一起参与探究。
实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和0.5mL溴乙烷振荡。
实验操作Ⅱ:将试管如图固定后,水浴加热。
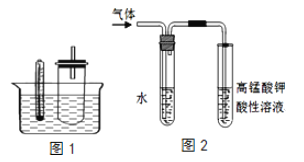
(1)据图1:用水浴加热而不直接用酒精灯加热的原因是________
(2)写出溴乙烷在NaOH水溶液中加热发生的化学反应方程式:________
(3)图2是为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,实验中需要检验的产物是:________ ,水的作用:________ ,实验现象是:________
【答案】使试管受热均匀 CH3CH2Br+NaOH![]() CH3CH2OH+NaBr 乙烯或CH2=CH2 除去乙烯中的乙醇,防止干扰乙烯的检验 酸性高锰酸钾溶液褪色
CH3CH2OH+NaBr 乙烯或CH2=CH2 除去乙烯中的乙醇,防止干扰乙烯的检验 酸性高锰酸钾溶液褪色
【解析】
(1)水浴加热,受热均匀;
(2)溴乙烷在NaOH水溶液中发生水解反应生成乙醇与溴化钠;
(3)溴乙烷在NaOH乙醇溶液中发生的是消去反应生成乙烯,乙烯能使酸性高锰酸钾褪色。
(1)据图1:用水浴加热而不直接用酒精灯加热的原因是使反应物均匀受热,控制温度在100℃以内,故答案为:使试管受热均匀;
(2)溴乙烷在NaOH水溶液中加热发生反应的化学方程式为:CH3CH2Br+NaOH![]() CH3CH2OH+NaBr;
CH3CH2OH+NaBr;
(3)证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,实验中需要检验的产物是CH2=CH2,由于乙醇易挥发,乙烯中混有的乙醇也能使酸性高锰酸钾溶液褪色,干扰乙烯的检验,所以图2中水的作用是:除去乙烯中的乙醇,防止干扰乙烯的检验,故答案为:乙烯或CH2=CH2;除去乙烯中的乙醇,防止干扰乙烯的检验;酸性高锰酸钾溶液褪色。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案