题目内容
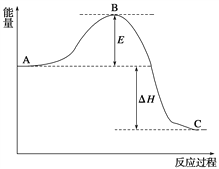
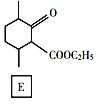
【题目】化合物E是一种药物合成中间体,其合成路线如下:
![]()
![]()
![]() D
D![]()
回答下列问题:
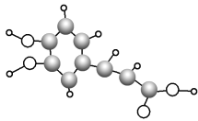
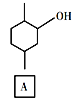
(1)A中的官能团名称是______。
(2)④的反应类型是______。
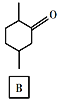
(3)B的分子式是______。
(4)D的结构简式是______。
(5)写出A到B的反应方程式______。
(6)H是A的同系物,含有六元碳环且比A少一个碳原子,则符合条件的H有______种(不考虑立体异构)。
【答案】羟基 酯化(或取代)反应 C8H14O 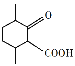 2
2![]() +O2
+O2![]() 2
2![]() +2H2O 5
+2H2O 5
【解析】
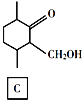
有机物A发生催化氧化,羟基转化为羰基生成B,B与甲醛发生加成反应是C,C中的羟基被酸性高锰酸钾氧化为羧基,则D的结构简式为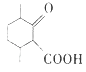 ,D与乙醇发生酯化反应生成E,据此分析解答。
,D与乙醇发生酯化反应生成E,据此分析解答。
(1)结合流程图中A的结构简式,A中官能团的名称为羟基;
(2)分析已知:反应④为D与乙醇发生酯化反应生成E,故反应类型为酯化(取代)反应;
(3)结合流程图中B的结构简式,每个节点为碳原子,每个碳原子可形成4个共价键,不足的键由氢原子补齐,则B的分子式是C8H14O;
(4)根据分析,D的结构简式是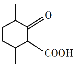 ;
;
(5)有机物A发生催化氧化,羟基转化为羰基生成B,反应方程式2![]() +O2
+O2![]() 2
2![]() +2H2O;
+2H2O;
(6)H是A的同系物,含有六元碳环且比A少一个碳原子,则H的结构中含有六元环、甲基和羟基(或醚基), 符合条件的H有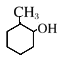 、
、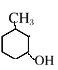 、
、![]() 、
、![]() 、
、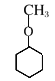 共5种。
共5种。

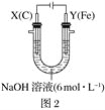
【题目】(1)100°C时,KW=1.0×10-12,在该温度下,测得0.1mol/L Na2A溶液pH=6。
①H2A在水溶液中的电离方程式为_____;
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,H2A溶液产生的H2_____(填“多”、“少”或“一样多”)。
(2)将0.4mol/L HA溶液与0.2mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-):
①混合溶液中c(A)_____c(HA)(填“>”、“<”或“=”,下同);
②混合溶液中c(HA)+c(A)_____0.2mol/L。
(3)已知在常温下测得浓度均为0.1mol/L的下列5种溶液的pH,如表所示:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①少量二氧化碳通入NaClO溶液中的离子方程式_____;
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是_____(填编号);
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c(CH3COO-)-c(CH3COOH)=_____mol/L(填准确数值)。