题目内容
20.恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g)(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值.
(2)反应达平衡时,混合气体的物质的量为32mol,其中NH3的物质的量分数为25%.计算原混合气体与平衡混合气体的压强之比(最简整数比,下同),即:P(始):P(平)=5:4.
(3)达到平衡时,求N2和H2的转化率之比,即:α(N2):α(H2)=1:2.
分析 (1)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
氮气起始物质的量=t时氮气物质的量+消耗氮气物质的量;
(2)计算氨气物质的量,根据方程式计算消耗氮气、氢气物质的量,结合平衡时混合气体总物质的量计算氢气起始物质的量,恒温恒容下,压强之比等于物质的量之比;
(3)结合(2)中计算结果进行解答.
解答 解:(1)(1)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
则a=3+13=16,
答:a的值为16;
(2)氨气物质的量为32mol×25%=8mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):16 b 0
变化量(mol):4 12 8
t时刻(mol):12 b-12 8
则12+b-12+8=32,解得b=24,
恒温恒容下,压强之比等于物质的量之比,则P(始):P(平)=(16+24)mol:32mol=5:4,
故答案为:5:4;
(3)α(N2):α(H2)=$\frac{4mol}{16mol}$:$\frac{12mol}{24mol}$=1:2,故答案为:1:2.
点评 本题考查化学平衡的计算,题目难度中等,注意三段式解题法在你化学平衡计算中应用.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案①硫化钠溶液 ②二氧化硫饱和溶液 ③硫酸铜溶液 ④硝酸银溶液 ⑤亚硫酸钠溶液.
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ①②④⑤ | D. | ②④⑤ |
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol/(L•min) | |
| B. | 6~10 min的平均反应速率:v(H2O2)<3.3×10-2 mol/(L•min) | |
| C. | 反应到6 min时,H2O2分解了50% | |
| D. | 反应到6 min时,c(H2O2)=0.30 mol/L |
| A. | 增加C的量 | |
| B. | 将容器的体积减小一半 | |
| C. | 保持体积不变,充入氮气使体系的压强增大 | |
| D. | 保持压强不变,充入氮气使体系的体积增大 |

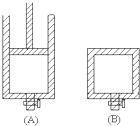 有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).
有两个容积相等的密闭容器A和B(如图)所示,A容器有一个可上下移动的活塞,能使容器保持恒压,B容器的容积不变.起始时这两个容器中分别充入等量按体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在400℃条件下,发生如下反应:2SO2(g)+O2(g)?2SO3(g).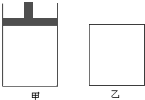 将4mol SO2与2mol O2的混合气分别置于容积相等的甲、乙两容器中,发生反应:2SO2(g)+O2(g)?2SO3(g);△H<0,在相同温度下使其均达到平衡状态.甲是恒压容器,乙是恒容容器.甲容器达到平衡状态时,测得混合气体的物质的量为4.2mol;乙容器经50s达到平衡状态.请回答:
将4mol SO2与2mol O2的混合气分别置于容积相等的甲、乙两容器中,发生反应:2SO2(g)+O2(g)?2SO3(g);△H<0,在相同温度下使其均达到平衡状态.甲是恒压容器,乙是恒容容器.甲容器达到平衡状态时,测得混合气体的物质的量为4.2mol;乙容器经50s达到平衡状态.请回答: