题目内容
【题目】FeSO4受热分解的化学方程式为:2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
请回答:
将FeSO4受热产生的气体按图示装置进行实验,证实含有SO2和SO3。能说明SO2存在的实验现象是_______;为测定BaSO4沉淀的质量,后续的操作步骤依次为____、洗涤、干燥、称量。
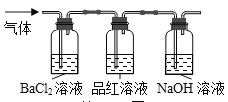
试剂一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)_______。
【答案】 品红溶液褪色 过滤 向固体成分中加入稀硫酸,取反应后溶液,滴加KSCN溶液,若有血红色出现,则表示溶液中存在Fe3+,产物中有Fe2O3存在
【解析】SO2具有漂白性,能说明SO2存在的实验现象是品红溶液褪色;为测定BaSO4沉淀的质量,后续的操作步骤依次为规律、洗涤、干燥、称量。固体是氧化铁,可以通过检验铁离子验证,即实验方案是向固体成分中加入稀硫酸,取反应后溶液,滴加KSCN溶液,若有血红色出现,则表示溶液中存在Fe3+,产物中有Fe2O3存在。

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目


