题目内容
下列说法正确的是:
A.在100℃、101kPa条件下,液态水的气化热为40. 69 kJ·mol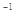 ,则 ,则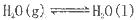 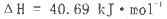 |
B.已知MgCO3的Ksp=6.82×10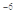 ,则所有含有固体MgCO3的溶液中,都有 ,则所有含有固体MgCO3的溶液中,都有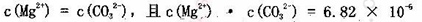 |
C.己知: 则可以计算出反应 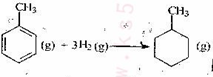 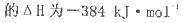 |
D.常温下,在0.10mol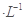 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的PH减小 |
D
解析试题分析:A、液态水的气化吸热,则气态水变为液态放热,△H<0,A错误;B、根据MgCO3的Ksp=6.82×10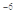 可知在溶液中有c(Mg2+)·c(CO32-)=6.82×10
可知在溶液中有c(Mg2+)·c(CO32-)=6.82×10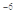 ,但c(Mg2+)与c(CO32-)不一定相等,B错误;C、苯环分子中无C=C和C-C键,是一种介于单键和双键之间的独特的键,不可用C-C和C=C键的数值进行计算反应热,C错误;D、加入少量NH4Cl晶体可抑制NH3·H2O的电离,正确。
,但c(Mg2+)与c(CO32-)不一定相等,B错误;C、苯环分子中无C=C和C-C键,是一种介于单键和双键之间的独特的键,不可用C-C和C=C键的数值进行计算反应热,C错误;D、加入少量NH4Cl晶体可抑制NH3·H2O的电离,正确。
考点:考查反应热的概念及计算、溶度积、苯的结构、弱电解质的电离等知识。

已知下列反应的热化学方程式为:
(1)C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
(2)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
(3)H2(g)+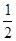 O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热ΔH为
| A.+488.3 kJ/mol | B.-488.3 kJ/mol | C.-244.15 kJ/mol | D.+244.15 kJ/mol |
已知298K时下述反应的有关数据:C(s)+1/2 O2(g)=CO(g) △H1 = -110.5kJ·mol-1
C(s)+O2 (g)=CO2(g), △H2= -393.5kJ/mol 则 C(s)+CO2(g)="2CO(g)" 的△H为
| A.283. kJ·mol-1 | B.+172.5 kJ·mol-1 |
| C.-172.5 kJ·mol-1 | D.-504 kJ·mol-1 |
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
| A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |
反应A(g)+B(g) 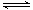 C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
| A.1molA与1molB充分反应后,能量变化为ΔE |
| B.加入催化剂后,反应加快,ΔE减小 |
| C.反应物的总键能小于生成物的总键能 |
| D.反应达到平衡时,升高温度,A的转化率增大 |
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ·mol-1,下列说法错误的是
| A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量 |
| B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ |
| C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量 |
| D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量 |
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是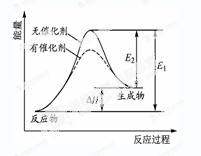
| A.该反应为放热反应 |
| B.催化剂能改变该反应的焓变 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
生活中每时每刻都发生着各种化学反应,下列反应不一定属于放热反应的是( )
| A.硫酸和氢氧化钡溶液的反应 | B.燃烧反应 |
| C.复分解反应 | D.中和反应 |
根据下面信息,判断下列叙述中正确的是 ( )
| A.1molH2和0.5molO2所具有的总能量低于1mol气态H2O所具有的总能量 |
| B.氢气跟氧气反应生成水的同时吸收能量 |
| C.1molH2跟1/2molO2反应生成1molH2O(l)释放能量一定是245kJ |
| D.2molH2(g)跟1molO2(g)反应生成2molH2O(g)释放能量490kJ |