题目内容
【题目】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液.
(1)上述十种物质中,属于电解质的有 , 属于非电解质的有 .
(2)有两种物质在水溶液中可发生反应,离子方程式为:H++OH﹣=H2O,该反应的化学方程式为 .
(3)除去③中少量②的操作是 , 化学方程式为 .
(4)现有100mL⑩溶液中含Fe3+5.6g,则溶液中SO42﹣的物质的量浓度是 .
(5)若在⑦中缓慢加入①的水溶液,产生的现象是 .
【答案】
(1)①②③⑥;④⑤
(2)HCl+KOH=H2O+KCl
(3)加热;HCl+KOH=H2O+KCl
(4)1.5mol/L
(5)先产生红褐色沉淀后沉淀溶解,溶液变黄色
【解析】解:(1)①液态氯化氢在水溶液中能导电,是电解质;
②NaHCO3在水溶液或者熔融状态下能够导电,是电解质;
③固体纯碱在水溶液或者熔融状态下能够导电,是电解质;
④葡萄糖在水溶液和熔融状态下都不能够导电,是非电解质;
⑤Ba(OH)2在熔融状态下能导电,是电解质;
⑥氢氧化钾在水溶液或者熔融状态下能够导电,是电解质;
⑦氢氧化铁胶体属于混合物 既不是电解质也不是非电解质;
⑧氨水属于混合物 既不是电解质也不是非电解质;
⑨空气属于混合物 既不是电解质也不是非电解质;
⑩硫酸铁溶液属于混合物 既不是电解质也不是非电解质;
故属于电解质的是:①②③⑥,非电解质的有:④⑤;
所以答案是:①②③⑥;④⑤;(2)离子方程式为:H++OH﹣═H2O,可表示强酸与强碱反应生成可溶性盐和水的离子反应,如HCl+KOH=H2O+KCl;
所以答案是:HCl+KOH=H2O+KCl;(3)根据碳酸钠加热不分解,碳酸氢钠加热分解得到碳酸钠、水、二氧化碳,所以除去固体纯碱中少量小苏打的操作是加热,方程式为:
所以答案是:加热;2NaHCO3 ![]() Na2CO3+H2O+CO2↑;(4)Fe3+的物质的量为
Na2CO3+H2O+CO2↑;(4)Fe3+的物质的量为 ![]() =0.1mol,溶液中2n(SO42﹣)=3n(Fe3+),则SO42﹣的物质的量为0.1mol×
=0.1mol,溶液中2n(SO42﹣)=3n(Fe3+),则SO42﹣的物质的量为0.1mol× ![]() =0.15mol,SO42﹣的物质的量浓度为
=0.15mol,SO42﹣的物质的量浓度为 ![]() =1.5mol/L;
=1.5mol/L;
所以答案是:1.5mol/L;(5)若在氢氧化铁胶体中缓慢加入盐酸,胶体发生聚沉,产生的现象是产生红褐色沉淀,继续加入盐酸,沉淀溶解得到黄色溶液,
所以答案是:先产生红褐色沉淀后沉淀溶解,溶液变黄色.

【题目】“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请回答下列问题:
(1)Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成 .
(2)Ⅱ、某稻壳灰的成分为:
组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
通过如图流程可由稻壳灰制备较纯净的二氧化硅.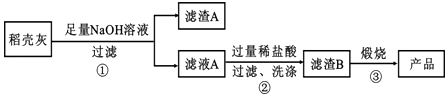
请回答下列问题:
根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有类.
(3)步骤①中涉及SiO2的离子反应方程式为 .
(4)滤渣A的成分有(填化学式)
(5)步骤②洗涤沉淀的方法是:
(6)步骤③反应的化学方程式为:;实验室进行步骤③用到的仪器有坩埚、、酒精灯、和三角架.
