题目内容
【题目】下表是元素周期表的一部分,按要求填空![]() 填元素符号或化学式
填元素符号或化学式![]() :
:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
![]() 写出下列元素的元素符号:①______②____________
写出下列元素的元素符号:①______②____________
![]() 在这些元素中,最活泼的金属元素是______,最活泼的非金属元素是______,最不活泼的元素是______.
在这些元素中,最活泼的金属元素是______,最活泼的非金属元素是______,最不活泼的元素是______.
![]() 在这些元素的最高价氧化物对应水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______.
在这些元素的最高价氧化物对应水化物中,酸性最强的是______,碱性最强的是______,呈两性的氢氧化物是______.
![]() 在③与④的单质中,化学性质较活泼的是______,判断依据是______;在⑧与的单质中,化学性质较为活泼的是______,判断依据是______.
在③与④的单质中,化学性质较活泼的是______,判断依据是______;在⑧与的单质中,化学性质较为活泼的是______,判断依据是______.
【答案】N F Ca K F Ar HClO4 KOH Al(OH)3 Na Na元素的金属性比Mg强 Cl2 氯元素的非金属性比溴强
【解析】
根据元素在元素周期表中的位置,可写出①~分别为N、F、Na、Mg、Al、Si、S、Cl、Ar、K、Ca、Br,然后根据元素周期律和元素化合物的性质答题即可。
(1)①②的元素符号分别为N、F、Ca;
(2)根据元素周期律我们可知,最活泼的金属元素应在周期表的左下角,最活泼的非金属元素应在周期表的右上角(除去稀有气体),最不活泼的元素应是稀有气体,故在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar;
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物应该在金属非金属的分界线上,是Al(OH)3;
(4)③与④为同周期主族金属元素,故Na元素的金属性比Mg强,所以单质较为活泼的是Na,⑧与为同主族非金属元素,故氯元素的非金属性比溴强,所以单质较为活泼的是氯气。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】甲醇是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
化学键 | H—H | C—O | C←=O | H—O | C—H |
E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
已知ΔH2=-58 kJ·mol-1,由此计算ΔH3=________kJ·mol-1。
(2)图1中能正确反映平衡常数K随温度变化关系的曲线为________(填曲线标记字母),其判断理由是___________________________________________________。
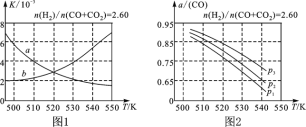
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而________(填“增大”或“减小”),其原因是______________________________________________________。图2中的压强由大到小为__________,其判断理由是___________________________________。