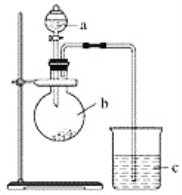
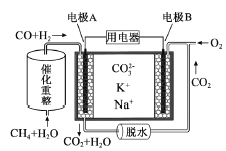
��Ŀ����
����Ŀ���ʻ���COS����ȫ����ѭ������Ҫ�м��壬Ҳ���л��ϳ��е���Ҫԭ�ϣ��ǻ�ѧ��������Ҫ���о�������֪��
����COS��g����H2��g��![]() H2S��g����CO��g�� ��Hl����17kJ��mol��
H2S��g����CO��g�� ��Hl����17kJ��mol��
����COS��g����H2O��g��![]() H2S��g����CO2��g�� ��H2����35kJ��mol��
H2S��g����CO2��g�� ��H2����35kJ��mol��
�ش��������⣺
(1)��ӦCO��g����H2O��g��![]() H2��g����CO2��g���ġ�H��________��
H2��g����CO2��g���ġ�H��________��
(2)�ڳ��д����ĺ�ѹ�ܱ������н��з�ӦI������ʼ�����n��H2����n��COS����m����ͬʱ���ڲ��COSת������m���¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��
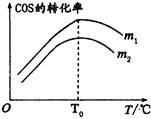 ��m1________m2�����������
��m1________m2�����������
���¶ȸ���T0ʱ��COSת���ʼ�С�Ŀ���ԭ��Ϊ_________��
A���и���Ӧ������
B����Ӧ�ġ�H����
C���������Խ��͡�
D���淴Ӧ��������ı���С������Ӧ��������ı���
(3)�ں��¡������ܱ������У����з�ӦI������˵������˵����ӦI�Ѵﵽƽ��״̬����___________��
A��c��H2S����c��CO�� B��v����H2����v����H2S��
C�������������ܶȱ��ֲ��� D�������л������ƽ��Ħ���������ֲ���
E��c��COS�����ֲ���
(4)ij�¶��£������Ϊ2 L�ĺ����ܱ�������ͨ��5 mol COS��g����5 molH2O��g����������Ӧ����5 min��Ӧ�ﵽƽ�⣬���COS��g����ת����Ϊ80����
�ٷ�Ӧ����ʼ��5 min�ڣ���H2SŨ�ȱ仯��ʾ��ƽ����Ӧ�ٶ�v��H2S����________��
�ڸ��¶��£�������Ӧ��ƽ�ⳣ��K��________��
������������ͬʱ������ʹ������Ӧ��COS��ƽ��ת���ʽ��ͣ�����ʹ��Ӧ���ʼӿ��������________��
A����С�����ݻ� B�������¶�
C����������� D������һ����H2O��g��
���𰸡�-18 kJ��mol �� A C B E 0.4mol/(Lmin) 16 B
��������
(1)���ݸ�˹���ɣ���Ӧ��-��Ӧ��ã�CO��g����H2O��g��![]() H2��g����CO2��g����H��-35+17=-18 kJ��mol���������������������-18 kJ��mol��
H2��g����CO2��g����H��-35+17=-18 kJ��mol���������������������-18 kJ��mol��
(2) ����ͬ�����£�n��H2��/n��COS��������COSת������������m1��m2������������������ǣ�����
��T0ǰ�������¶�������Ӧ���ʼӿ���COSת�����������¶ȸ���T0ʱ�������Ļ��Խ�������������Ӧ���淴Ӧ��������ı�����������Ӧ��������ı��������п��ܵ���COSת���ʼ�С���ʱ����¶���������������������ǣ�A C ��
(3)��Ӧ��COS��g����H2��g��![]() H2S��g����CO��g�� ��Hl����17kJ��mol��
H2S��g����CO��g�� ��Hl����17kJ��mol��
A��c��H2S����c��CO����û��ָ����Ӧ���ʽ��еķ��������ж���ӦI�Ѵﵽƽ��״̬��������
B��v����H2����v����H2S����ָ�����淴Ӧ���ʵķ���������������֮�Ⱥ�ϵ�������ȣ������ж���ӦI�Ѵﵽƽ��״̬����ȷ��
C����Ӧǰ����������������䣬������������䣬���������������ܶ�ʼ�ձ��ֲ��䣬���ж���ӦI�Ѵﵽƽ��״̬��������
D����Ӧǰ����������������䣬��Ӧǰ�����������Ҳ���ֲ��䣬����![]() =m������/n(��) ��֪�������л������ƽ��Ħ������ʼ�ձ��ֲ��䣬���ж���ӦI�Ѵﵽƽ��״̬��������
=m������/n(��) ��֪�������л������ƽ��Ħ������ʼ�ձ��ֲ��䣬���ж���ӦI�Ѵﵽƽ��״̬��������
E��c��COS�����ֲ��䣬�����ж���ӦI�Ѵﵽƽ��״̬����ȷ��
��������������ѡB E��
(4) COS��g����H2O��g��![]() H2S��g����CO2��g��
H2S��g����CO2��g��
��ʼ�� 5 5 0 0
�仯�� 5��80�� 5��80�� 5��80�� 5��80��
5 min���� 1 1 4 4
�ٷ�Ӧ����ʼ��5 min�ڣ���H2SŨ�ȱ仯��ʾ��ƽ����Ӧ�ٶ�v��H2S����4/(2��5)=0.4mol/(Lmin)���������������������0.4mol/(Lmin)��
�ڸ��¶��£���Ӧ�ﵽƽ���c(COS)=1/2=0.5mol/L��c(H2O )=1/2=0.5mol/L��c(H2S)=4/2=2mol/L��c( CO2)=4/2=2mol/L��ƽ�ⳣ��K��2��2/0.5��0.5=16���������������������16��
��A����Ϊ��Ӧǰ�������������С�����ݻ� ������ѹǿ����Ӧ���ʼӿ���ƽ�ⲻ�ƶ� ��COS��ƽ��ת���ʲ��䣬����
B���÷�ӦΪ���ȷ�Ӧ�������¶���ƽ�����������ʼӿ���COS��ƽ��ת���ʼ�С����ȷ��
C���������������С������Ũ����ƽ��������COS��ƽ��ת�������������ʼ���������
D������һ����H2O��g����ƽ����������Ӧ���ʼӿ���COS��ƽ��ת����������
��������������ѡB��

����Ŀ������ˮ�Ǻϳ�ϩ���ij��÷���,ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ�����£�

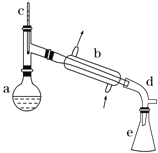
�����õ����й��������£�
��Է������� | �ܶ�/(g/cm3) | �е�/�� | �ܽ��� | |
������ | 100 | 0.9618 | 161 | ����ˮ |
����ϩ | 82 | 0.8102 | 83 | ������ˮ |
�ϳɷ�Ӧ��
��a�м���20g��������2СƬ���Ƭ����ȴ��������������1mLŨH2SO4 ��b��ͨ����ȴˮ��ʼ��������a������������¶Ȳ�����90�档
�����ᴿ��
��Ӧ�ֲ��ﵹ�����©���У��ֱ���������5%̼������Һ��ˮϴ�ӣ�����������ˮCaCl2����������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������ô�������ϩ10g��
�ش��������⣺
��1��װ��b��������_____��
��2���������Ƭ��������_____���������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������_______(����ȷ�𰸱��)��
A���������� B����ȴ�� C�����貹�� D����������
��3����ʵ���������ײ���������Ľṹ��ʽΪ_______��
��4����Һ©����ʹ��ǰ����ϴ�ɾ���________����ʵ���������в���Ӧ�ôӷ�Һ©����________����Ͽڵ��������¿ڷų�������
��5�������ᴿ�����м�����ˮ�Ȼ��Ƶ�Ŀ����_____��
��6���ڻ���ϩ�ֲ�����������У��������õ���������________������ȷ�𰸱�ţ���
A��Բ����ƿ B���¶ȼ� C������ƿ D������������ E��������
��7����ʵ�������õĻ���ϩ�IJ�����________ (����ȷ�𰸵ı��)��
A��41% B��50% C��61% D��70%