题目内容
【题目】Ⅰ.A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.16 g·Lˉ1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
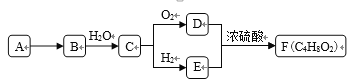
请回答:
(1)有机物D中含有的官能团名称是________。
(2)有机物A在高温下转化为B的化学方程式是_________________。
(3)下列说法正确的是________。
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
Ⅱ.已知:当一个碳原子上连有两个羟基时易发生下列转化:
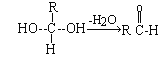
根据下图所示的反应路线及所给的信息填空。
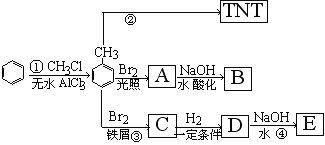
B遇石蕊试液变红,C的苯环上一元取代物只有2种同分异构体。
回答下列问题:
(1)A的结构简式为_____________,D的结构简式为_________________。
(2)③的反应类型为_________。
(3)反应②的化学方程式为____________________________。
【答案】羧基 ![]() BD
BD ![]()
![]() 取代反应
取代反应 
【解析】
Ⅰ.A是天然气的主要成分,则A为CH4;已知烃B在标准状况下的密度为1.16gL-1,则B的摩尔质量为:M(B)=22.4L/mol×1.16gL-1≈26g/mol;C能发生银镜反应,则C分子中含有醛基;F为有浓郁香味,不易溶于水的油状液体,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH、C为CH3CHO;B与水反应生成乙醛,且B的摩尔质量为26g/mol,则B为CH≡CH,据此进行解答;
Ⅱ.![]() 和CH3Cl在催化剂作用下发生取代反应生成
和CH3Cl在催化剂作用下发生取代反应生成![]() ;甲苯和浓硫酸、浓硝酸的混合液加热生成2,4,6-三硝基甲苯(
;甲苯和浓硫酸、浓硝酸的混合液加热生成2,4,6-三硝基甲苯(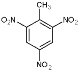 );甲苯与Br2在光照条件下发生取代反应生成A,A在NaOH水溶液中发生水解反应生成的B遇石蕊试液变红,可知B为
);甲苯与Br2在光照条件下发生取代反应生成A,A在NaOH水溶液中发生水解反应生成的B遇石蕊试液变红,可知B为![]() ,A为
,A为![]() ;
;![]() 和液溴在Fe粉作催化剂的作用下生成C,C的苯环上一元取代物只有2种同分异构体,则C为
和液溴在Fe粉作催化剂的作用下生成C,C的苯环上一元取代物只有2种同分异构体,则C为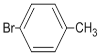 ,C再与H2发生加成反应生成
,C再与H2发生加成反应生成![]() ,
,![]() 再在NaOH溶液中发生水解反应生成的E为
再在NaOH溶液中发生水解反应生成的E为![]() ,据此分析解题。
,据此分析解题。
Ⅰ.(1)D的结构简式为D为CH3COOH,其含有官能团为羧基;
(2)A为CH4,B为CH≡CH,CH4在高温下转化为CH≡CH的化学方程式是![]() ;
;
(3)A.E为CH3CH2OH,乙醇与金属钠反应不如水与金属钠反应剧烈,故A错误;
B.D为CH3COOH、E为CH3CH2OH、F为CH3COOC2H5,乙酸与碳酸钠生成气体,乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于碳酸钠溶液,所以可用饱和Na2span>CO3溶液鉴别三者,故B正确;
C.实验室制备乙酸乙酯时,浓硫酸为催化剂和吸水剂,不体现氧化性,故C错误;
D.有机物C为CH3CHO,CH3CHO中含有官能团醛基,醛基能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化,故D正确;
故答案为:BD;
Ⅱ.(1)由分析知:A的结构简式为![]() ,D的结构简式为
,D的结构简式为![]() ;
;
(2)反应③为![]() 和液溴在Fe粉作催化剂的作用下发生取代反应生成
和液溴在Fe粉作催化剂的作用下发生取代反应生成 ;
;
(3)反应②为甲苯和浓硫酸、浓硝酸的混合液加热生成TNT,反应的化学方程式为 。
。

【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
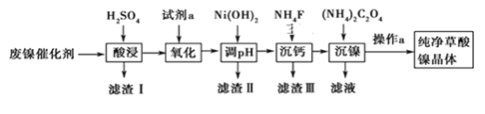
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)在酸浸过程中会适当增大酸的浓度并不断快速搅拌,目的是______________。
(2)写出“沉镍”时发生反应的离子方程式:______________________________,当Ca2+沉淀完全时,溶液中 c(F-)> ________mol·L-1(写出计算式即可)。
(3)试剂a是一种绿色氧化剂,写出“氧化”时反应的化学反应方程式:_______________________________。
(4)操作a的内容包括过滤,洗涤,干燥。请用简洁语言描述洗涤的方法是__________________________。
(5)“调pH”时pH的调控范围为______≤PH<6.8。