题目内容
15.下列关于有机物的说法错误的是( )| A. | 乙烯和苯都能与溴水反应 | |
| B. | 乙烷和丙烯的物质的量共1mol,完全燃烧都生成3molH2O | |
| C. | 苯和乙烯都能与H2发生加成反应 | |
| D. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
分析 A、乙烯含有碳碳双键能与溴水发生加成反应,苯与溴水不反应,但可以萃取溴水中的溴;
B、1mol乙烷和丙烯的混合物中,不论以何种比例混合,H原子数为6mol,据此解答即可;
C、苯与乙烯都能发生加成反应;
D、苯不含碳碳双键,不能使酸性高锰酸钾褪色,但苯能燃烧.
解答 解:A、乙烯与溴水发生加成反应使溴水褪色,苯萃取溴水中的溴使溴水褪色,苯不与溴水反应,故A错误;
B、1mol乙烷和丙烯的混合物中,不论以何种比例混合,H原子数为6mol,产物均为3mol水,故B正确;
C、乙烯与氢气加成生成乙烷,苯与氢气加成生成环己烷,两者都能与氢气发生加成反应,故C正确;
D、苯中的化学键介于单键与双键中的一种特殊键,不能使KMnO4溶液褪色,苯能燃烧,属于氧化反应,故D错误;故选AD.
点评 本题主要考查的是苯与乙烯的性质,难度不大,掌握烃类的燃烧也属于氧化反应是解决本题的关键.

练习册系列答案
相关题目
11.下列说法中不正确的是( )
| A. | 在甲、乙两烧杯的溶液中,共含有Cu2+、K-、H+、Cl-、CO32-、OH-六种离子.已知甲烧杯的溶液含其中3种离子并呈蓝绿色,则乙烧杯的溶液中含有的3种离子是:K+、OH-、CO32- | |
| B. | 常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大量共存 | |
| C. | 在含有HCO3-、SO32-、S2-、CH3COO-四种阴离子的溶液中加入足量的BaO2固体后,CH3COO-浓度变化最小 | |
| D. | 常温下水电离出的c(OH-)=10-10的溶液中:Na+、ClO-、S2-、NH4+不能大量共存 |
2.下列变化中,不需要破坏化学键的是( )
| A. | NO与O2反应 | B. | 碘加热升华 | C. | 氯酸钾加热分解 | D. | 氯化钠溶于水 |
20.下列物质性质变化的比较,不正确的是( )
| A. | 酸性强弱:HIO4>HBrO4 | B. | 原子半径大小 Na>S>O | ||
| C. | 碱性强弱KOH>NaOH | D. | 金属性强弱Na>Mg>Al |
 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1:1的化合物N是常见的有机溶剂. ,E的基态原子的外围电子排布式为3d24s2.
,E的基态原子的外围电子排布式为3d24s2.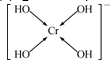 .(若有配位键,用箭号表示)
.(若有配位键,用箭号表示)