题目内容
【题目】工业上利用铬铁矿(FeO![]() Cr2O3)冶炼铬的工艺流程如下:
Cr2O3)冶炼铬的工艺流程如下:

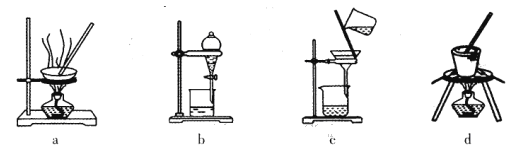
(1)实验室焙烧铬铁矿可选用的装置是__________(填序号)。
(2)完成下列化学方程式(在横线上填写物质的化学式及计量数):4CrO42-+6S+7H2O=4Cr(OH)3↓+3S2O32-+_____________。
(3)操作I包括过滤与洗涤,过滤需要的玻璃仪器有:__________________________。
(4)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,写出Cr(OH)3溶于氢氧化钠溶液的
离子方程式_________________________________。
(5)由Cr2O3冶炼Cr的化学方程式为________________________。
【答案】 d 2OH- 烧杯、漏斗、玻璃棒 Cr(OH)3+ OH- = CrO2- + 2H2O Cr2O3+2Al ![]() 2Cr+ Al2O3
2Cr+ Al2O3
【解析】本题主要考查化学实验基本操作、方程式配平、方程式书写、金属冶炼等。(1)实验室焙烧铬铁矿需要在坩埚中完成,因此实验室焙烧铬铁矿可选用的装置是d;(2)根据电荷守恒和原子守恒可知,该微粒是2OH-;(3)过滤需要的玻璃仪器有烧杯、漏斗、玻璃棒;(4)氢氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水,Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。因此Cr(OH)3溶于浓氢氧化钠溶液反应生成的是NaCrO2和水,反应的离子方程式为Cr(OH)3+ OH-= CrO2-+2H2O;(5)根据流程信息可知:Cr2O3加入铝粉即得Cr,其化学方程式为Cr2O3+ 2Al![]() 2Cr + Al2O3。
2Cr + Al2O3。

【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是(_____)

选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
C. | 硫酸亚铁溶液 | 过氧化钠 | 形成黄色溶液 |
D. | 硫酸铁溶液 | 氢硫酸溶液 | 产生黄色浑浊 |
A. A B. B C. C D. D
