题目内容
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
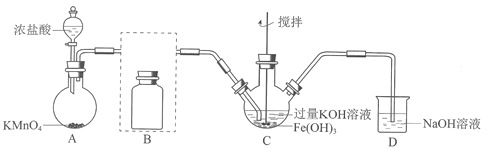
①A为氯气发生装置。A中反应方程式是________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。_______
③C中得到紫色固体和溶液。C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O,另外还有________________。
2K2FeO4+6KCl+8H2O,另外还有________________。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________。
②根据K2FeO4的制备实验得出:氧化性Cl2________![]() (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和![]() 的氧化性强弱关系相反,原因是________________。
的氧化性强弱关系相反,原因是________________。
③资料表明,酸性溶液中的氧化性![]() >
>![]() ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性![]() >
>![]() 。若能,请说明理由;若不能,进一步设计实验方案。
。若能,请说明理由;若不能,进一步设计实验方案。
理由或方案:________________。
【答案】 2KMnO4+16HCl![]() 2MnCl2+2KCl +5Cl2↑+8H2O
2MnCl2+2KCl +5Cl2↑+8H2O  Cl2+2OH
Cl2+2OH![]() Cl+ClO+H2O Fe3+ 4FeO42+20H+
Cl+ClO+H2O Fe3+ 4FeO42+20H+![]() 4Fe3++3O2↑+10H2O 排除ClO的干扰 > 溶液的酸碱性不同 若能,理由:FeO42在过量酸的作用下完全转化为Fe3+和O2,溶液浅紫色一定是MnO4的颜色(若不能,方案:向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色)
4Fe3++3O2↑+10H2O 排除ClO的干扰 > 溶液的酸碱性不同 若能,理由:FeO42在过量酸的作用下完全转化为Fe3+和O2,溶液浅紫色一定是MnO4的颜色(若不能,方案:向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色)
【解析】分析:(1)KMnO4与浓盐酸反应制Cl2;由于盐酸具有挥发性,所得Cl2中混有HCl和H2O(g),HCl会消耗Fe(OH)3、KOH,用饱和食盐水除去HCl;Cl2与Fe(OH)3、KOH反应制备K2FeO4;最后用NaOH溶液吸收多余Cl2,防止污染大气。
(2)①根据制备反应,C的紫色溶液中含有K2FeO4、KCl,Cl2还会与KOH反应生成KCl、KClO和H2O。
I.加入KSCN溶液,溶液变红说明a中含Fe3+。根据题意K2FeO4在酸性或中性溶液中快速产生O2,自身被还原成Fe3+。
II.产生Cl2还可能是ClO-+Cl-+2H+=Cl2↑+H2O,即KClO的存在干扰判断;K2FeO4微溶于KOH溶液,用KOH洗涤除去KClO、排除ClO-的干扰,同时保持K2FeO4稳定存在。
②根据同一反应中,氧化性:氧化剂![]() 氧化产物。对比两个反应的异同,制备反应在碱性条件下,方案II在酸性条件下,说明酸碱性的不同影响氧化性的强弱。
氧化产物。对比两个反应的异同,制备反应在碱性条件下,方案II在酸性条件下,说明酸碱性的不同影响氧化性的强弱。
③判断的依据是否排除FeO42-的颜色对实验结论的干扰。
详解:(1)①A为氯气发生装置,KMnO4与浓盐酸反应时,锰被还原为Mn2+,浓盐酸被氧化成Cl2,KMnO4与浓盐酸反应生成KCl、MnCl2、Cl2和H2O,根据得失电子守恒和原子守恒,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。
②由于盐酸具有挥发性,所得Cl2中混有HCl和H2O(g),HCl会消耗Fe(OH)3、KOH,用饱和食盐水除去HCl,除杂装置B为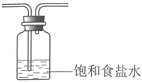 。
。
③ C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,还有Cl2与KOH的反应,Cl2与KOH反应的化学方程式为Cl2+2KOH=KCl+KClO+H2O,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O。
(2)①根据上述制备反应,C的紫色溶液中含有K2FeO4、KCl,还可能含有KClO等。
i.方案I加入KSCN溶液,溶液变红说明a中含Fe3+。但Fe3+的产生不能判断Kspan>2FeO4与Cl-发生了反应,根据题意K2FeO4在酸性或中性溶液中快速产生O2,自身被还原成Fe3+,根据得失电子守恒、原子守恒和电荷守恒,可能的反应为4FeO42-+20H+=3O2↑+4Fe3++10H2O。
ii.产生Cl2还可能是ClO-+Cl-+2H+=Cl2↑+H2O,即KClO的存在干扰判断;K2FeO4微溶于KOH溶液,用KOH溶液洗涤的目的是除去KClO、排除ClO-的干扰,同时保持K2FeO4稳定存在。
②制备K2FeO4的原理为3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,在该反应中Cl元素的化合价由0价降至-1价,Cl2是氧化剂,Fe元素的化合价由+3价升至+6价,Fe(OH)3是还原剂,K2FeO4为氧化产物,根据同一反应中,氧化性:氧化剂![]() 氧化产物,得出氧化性Cl2
氧化产物,得出氧化性Cl2![]() FeO42-;方案II的反应为2FeO42-+6Cl-+16H+=2Fe3++3Cl2↑+8H2O,实验表明,Cl2和FeO42-氧化性强弱关系相反;对比两个反应的条件,制备K2FeO4在碱性条件下,方案II在酸性条件下;说明溶液的酸碱性的不同影响物质氧化性的强弱。
FeO42-;方案II的反应为2FeO42-+6Cl-+16H+=2Fe3++3Cl2↑+8H2O,实验表明,Cl2和FeO42-氧化性强弱关系相反;对比两个反应的条件,制备K2FeO4在碱性条件下,方案II在酸性条件下;说明溶液的酸碱性的不同影响物质氧化性的强弱。
③该小题为开放性试题。若能,根据题意K2FeO4在足量H2SO4溶液中会转化为Fe3+和O2,最后溶液中不存在FeO42-,溶液振荡后呈浅紫色一定是MnO4-的颜色,说明FeO42-将Mn2+氧化成MnO4-,所以该实验方案能证明氧化性FeO42-![]() MnO4-。(或不能,因为溶液b呈紫色,溶液b滴入MnSO4和H2SO4的混合溶液中,c(FeO42-)变小,溶液的紫色也会变浅;则设计一个空白对比的实验方案,方案为:向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色)。
MnO4-。(或不能,因为溶液b呈紫色,溶液b滴入MnSO4和H2SO4的混合溶液中,c(FeO42-)变小,溶液的紫色也会变浅;则设计一个空白对比的实验方案,方案为:向紫色溶液b中滴加过量稀H2SO4,观察溶液紫色快速褪去还是显浅紫色)。