题目内容
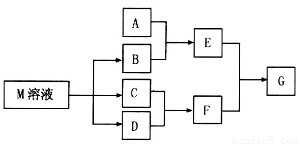
下图为某些常见物质之间的转化关系。已知A为有色气体单质, 反应②是实验室制取气体F的常用方法。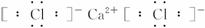
请按要求填空:
(1)E的电子式是_______________,B中含有的化学键类型有_______________。
(2)反应②的化学方程式是_____________________________________________。
(3)反应①在工业上有重要的用途,其化学方程式是______________________________。
(4)取一试管A气体倒置于水槽中光照足够长的时间,(假设溶质不扩散到试管外,气体体积按标准状况下计算)所得溶液的物质的量浓度为______________________________。
(5)G为一元弱酸,设G的化学式为HX,常温下如果取0.1 mol·L-1HX溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液总体积等于两溶液体积之和),测得混合溶液的pH=8。
求出混合溶液中下列算式的精确计算结果:
c(Na+)-c(X-)=__________________mol·L-1
(1)![]() 离子键、共价键
离子键、共价键
(2)Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(3)2Ca(OH)2+2Cl2====CaCl2+Ca(ClO)2+2H2O
(4)1/5.6 mol·L-1
(5)9.9×10-7
解析:无机推断题的关键是找关键点:(1)A为有色气体单质可推知为氯气;(2)B、C加热生成F、E和水是实验室制气体F的方法,且F与I产生白烟,可推知F为NH3;(3)Cl2和B生成D、E和水,故B为Ca(OH)2,其余各物质依次推出。
(4)设Cl2的体积为V,据方程式:Cl2+2H2O====2HCl+O2可求出HCl的物质的量,溶液的体积为V的一半,可求物质的量浓度。
(5)据电荷守恒c(Na+)-c(X-)=c(OH-)-c(H+)=(

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案

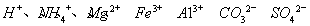
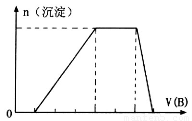

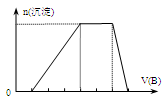
 (2)SO2的排放是造成酸雨的主要因素。某地区酸雨
(2)SO2的排放是造成酸雨的主要因素。某地区酸雨