题目内容
国家环保总局“2006年环境监测公报”指出,减少SO2的排放和生活废水的处理是我国“十一五”期间环境保护的主要任务。请回答下列问题:
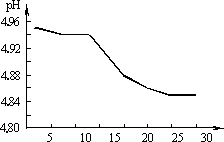
(1)SO2的排放是造成酸雨的主要因素。某地区酸雨pH随时间的变化如下图所示。请用化学方程式表示该地区酸雨pH随时间增加而减小的原因______________________________。

(2)新型氨法烟气脱硫技术采用氨吸收烟气中SO2生成亚硫酸铵和亚硫酸氢铵,再用一定量的磷酸进行反应,在反应回收SO2后的混合物中通入适量的氨气得到一种产品。该技术的优点是_______________________________________________________。
(3)为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及的化学反应为:SO2+2CO====2CO2+![]() Sx、CO+
Sx、CO+![]() Sx====COS、2COS+SO2====2CO2+
Sx====COS、2COS+SO2====2CO2+![]() Sx。其中COS分子的空间构型为______________。
Sx。其中COS分子的空间构型为______________。
(4)生活污水中含大量细小的悬浮物,可加入某些物质使之聚集成较大的颗粒而沉淀。请你举一种常见的能使生活污水中悬浮物聚沉的物质,其化学式为_____________。若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在硝化细菌的作用下将![]() 氧化为
氧化为![]() :
:![]() +2O2====
+2O2====![]() +2H++H2O,然后加入甲醇,
+2H++H2O,然后加入甲醇,![]() 和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式__________________________。
和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式__________________________。
(1)2H2SO3+O2====2H2SO4
(2)既能回收利用SO2,又能得到复合肥磷铵
(3)直线形
(4)KAl(SO4)2·12H2O或FeSO4·7H2O,6![]() +5CH3OH+6H+====3N2↑+5CO2↑+13H2O
+5CH3OH+6H+====3N2↑+5CO2↑+13H2O
解析:本题的起点比较高,但经过认真分析,所考查知识点都是比较简单的,属于中等题。(1)酸雨pH小于7的原因是溶解了亚硫酸,随着时间越长,亚硫酸逐渐被氧化成硫酸,pH进一步变小。(2)此技术的优点是通过磷酸和亚硫酸铵、亚硫酸氢铵反应,既生成SO2,又能得到复合肥磷铵。(3)COS分子中只是相当于将二氧化碳分子中一个氧原子换成硫原子,S、O原子在周期表中位于同一主族,结构相似,故仍为直线形。(4)常见的使生活污水中悬浮物聚沉的物质是明矾。![]() 和甲醇转化为两种无毒气体,根据物质组成元素应为N2和CO2,方程式可得。
和甲醇转化为两种无毒气体,根据物质组成元素应为N2和CO2,方程式可得。

| |||||||||||||||||||||||||||||