题目内容
由短周期元素形成的六种微粒,有四种离子和两种分子,其中A,E是由非金属元素的原子构成的阳离子,这六种微粒均具有10个电子.它们的相互关系如下:
①A,B两种离子在加热条件下,可生成C,D两种分子;
②C是常温下呈气态的分子,遇HCl时可冒白烟;
③E,B两种离子相互作用可生成2个D的分子;
④含F微粒的溶液,遇B会产生白色沉淀W,B过量时,W又可溶解变为无色溶液;在此无色溶液中加入E时,又产生白色沉淀W;E过量时,W又转化为F.
根据以上关系,回答下列各问:
(1)写出A+B C+D的化学方程式________.
C+D的化学方程式________.
(2)C遇HCl冒白烟的化学方程式________.
(3)写出E,B反应生成2D的离子方程式________.
(4)F微粒的符号是________,白色沉淀W的化学式是________,W溶于B的离子方程式为________.
答案:
解析:
解析:
|
(1) (2)NH3+HCl=NH4Cl (3)H3O++OH-=2H2O (4)Al3+,Al(OH)3,Al(OH)3+OH-= |

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
 +OH-
+OH- NH3+H2O
NH3+H2O +2H2O
+2H2O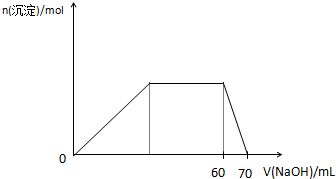 (2011?湖北模拟)X、Y、Z、M、N、K是由短周期元素构成的微粒,其中X、Y、Z是阳离子,M、N是中性分子,K是阴离子,它们具有下列结构特点和性质:
(2011?湖北模拟)X、Y、Z、M、N、K是由短周期元素构成的微粒,其中X、Y、Z是阳离子,M、N是中性分子,K是阴离子,它们具有下列结构特点和性质:
