��Ŀ����
A��B��C��D��E���ɶ�����Ԫ����ɵ����ֳ������ʣ���֪��
�ٳ����¾�����̬������B��C��FΪ���ʣ�
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣻
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ�
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ��
�ش��������⣺
��1��A�ĵ���ʽ�� ��ʵ������ȡB�Ļ�ѧ����ʽΪ ��
��2��A��ˮ��Һ�ʼ��Ե�ԭ���� ����ϻ�ѧ����˵�������������ʵ���Ũ�ȡ��������A��D��Һ��ϣ�������Һ������Ũ���ɴ�С��������Ϊ ��
��3��һ��������A��F��Ӧ������C��һ����ɫ��ζҺ�壬�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ ��
��4�����C��B�����ʵ�Ԫ�أ���ԭ�Ӹ���1��3�γɻ�����G��G��һ�ֵ���ɫҺ�壬��ˮ������ˮ�������һ�־���Ư���Ե����ʣ�д����Ӧ�ķ���ʽ ���÷�Ӧ˵�����C��B�����ʵ�Ԫ���зǽ����Խ�ǿ���� ������Ԫ�ط��ţ�
�ٳ����¾�����̬������B��C��FΪ���ʣ�
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣻
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ�
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ��
�ش��������⣺
��1��A�ĵ���ʽ��
��2��A��ˮ��Һ�ʼ��Ե�ԭ����
��3��һ��������A��F��Ӧ������C��һ����ɫ��ζҺ�壬�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ
��4�����C��B�����ʵ�Ԫ�أ���ԭ�Ӹ���1��3�γɻ�����G��G��һ�ֵ���ɫҺ�壬��ˮ������ˮ�������һ�־���Ư���Ե����ʣ�д����Ӧ�ķ���ʽ
�������ٳ����¾�����̬������B��C��FΪ���ʣ�
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ�ж�EΪNO��C��FΪN2��O2��
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣬�ƶ�BΪCl2��
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ��ƶ�AΪNH3��CΪN2��FΪO2��DΪHCl��
�������������жϵõ�ABCDEF�ֱ�ΪNH3��Cl2��N2��HCl��NO��O2��
�������ʻش����⣮
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ�ж�EΪNO��C��FΪN2��O2��
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣬�ƶ�BΪCl2��
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ��ƶ�AΪNH3��CΪN2��FΪO2��DΪHCl��
�������������жϵõ�ABCDEF�ֱ�ΪNH3��Cl2��N2��HCl��NO��O2��
�������ʻش����⣮
����⣺�ٳ����¾�����̬������B��C��FΪ���ʣ�
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ�ж�EΪNO��C��FΪN2��O2��
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣬�ƶ�BΪCl2��
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ��ƶ�AΪNH3��CΪN2��FΪO2��DΪHCl��
�������������жϵõ�ABCDEF�ֱ�ΪNH3��Cl2��N2��HCl��NO��O2��
��1��AΪ��������ԭ�Ӻ�������ԭ���γɹ��ۼ�������ʽΪ�� ��ʵ�����Ʊ����������ö������̺�Ũ������ȷ�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��
��ʵ�����Ʊ����������ö������̺�Ũ������ȷ�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O��
�ʴ�Ϊ�� MnO2+4HCl��Ũ��
MnO2+4HCl��Ũ��
MnCl2+Cl2��+2H2O��
��2��A��Һ��һˮ�ϰ���Һ��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ�NH3?H2O?NH4++OH-���������ʵ���Ũ�ȡ��������A��D��Һ��ϣ�������Һ������Ϊ�Ȼ�泥���Һ��笠�����ˮ�⣬��Һ�����ԣ���Һ������Ũ���ɴ�С��������Ϊc��Cl-����c��NH4+����c��H+����c��OH-����
�ʴ�Ϊ��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������������������ӣ�NH3?H2O?NH4++OH-��c��Cl-����c��NH4+����c��H+����c��OH-����
��3��һ��������AΪ������FΪһ��Ӧ������CΪ������һ����ɫ��ζҺ��Ϊˮ����Ӧ�Ļ�ѧ����ʽΪ��4NH3+3O2=2N2+6H2O���÷�Ӧ�������������뻹ԭ�����������ʵ���֮��Ϊ3��4��
�ʴ�Ϊ��3��4��
��4�����C��B�����ʵ�Ԫ��Ϊ��Ԫ�غ���Ԫ�أ���ԭ�Ӹ���1��3�γɻ�����GΪNCl3��G��һ�ֵ���ɫҺ�壬��ˮ������ˮ�������һ�־���Ư���Ե������ж�ΪHClO����һ������Ϊ��������Ӧ�Ļ�ѧ����ʽΪ��NCl3+3H2O=NH3+3HClO������Ԫ�ػ��ϼ۱仯��֪��Ԫ�ػ��ϼ۽���Ϊ-3�ۣ���Ԫ�ػ��ϼ�����Ϊ+1�ۣ����Ե�Ԫ�صķǽ�����ǿ����Ԫ�أ�
�ʴ�Ϊ��NCl3+3H2O=NH3+3HClO��N��
��C��F�ڷŵ������·�Ӧ����E��E��������ɫ�ж�EΪNO��C��FΪN2��O2��
��ʵ������ȡBʱ�����ű���ʳ��ˮ���ռ��ɼ���B��ˮ�е��ܽ⣬�ƶ�BΪCl2��
��A��B��Ӧ����C��D��A��ˮ��Һ�ʼ��ԣ�D��ˮ��Һ�����ԣ��ƶ�AΪNH3��CΪN2��FΪO2��DΪHCl��
�������������жϵõ�ABCDEF�ֱ�ΪNH3��Cl2��N2��HCl��NO��O2��
��1��AΪ��������ԭ�Ӻ�������ԭ���γɹ��ۼ�������ʽΪ��
 ��ʵ�����Ʊ����������ö������̺�Ũ������ȷ�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��
��ʵ�����Ʊ����������ö������̺�Ũ������ȷ�Ӧ���ɣ���Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��
| ||
�ʴ�Ϊ��
 MnO2+4HCl��Ũ��
MnO2+4HCl��Ũ��
| ||
��2��A��Һ��һˮ�ϰ���Һ��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������������������ӣ���Һ�ʼ��ԣ�NH3?H2O?NH4++OH-���������ʵ���Ũ�ȡ��������A��D��Һ��ϣ�������Һ������Ϊ�Ȼ�泥���Һ��笠�����ˮ�⣬��Һ�����ԣ���Һ������Ũ���ɴ�С��������Ϊc��Cl-����c��NH4+����c��H+����c��OH-����
�ʴ�Ϊ��������ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������������������ӣ�NH3?H2O?NH4++OH-��c��Cl-����c��NH4+����c��H+����c��OH-����
��3��һ��������AΪ������FΪһ��Ӧ������CΪ������һ����ɫ��ζҺ��Ϊˮ����Ӧ�Ļ�ѧ����ʽΪ��4NH3+3O2=2N2+6H2O���÷�Ӧ�������������뻹ԭ�����������ʵ���֮��Ϊ3��4��
�ʴ�Ϊ��3��4��
��4�����C��B�����ʵ�Ԫ��Ϊ��Ԫ�غ���Ԫ�أ���ԭ�Ӹ���1��3�γɻ�����GΪNCl3��G��һ�ֵ���ɫҺ�壬��ˮ������ˮ�������һ�־���Ư���Ե������ж�ΪHClO����һ������Ϊ��������Ӧ�Ļ�ѧ����ʽΪ��NCl3+3H2O=NH3+3HClO������Ԫ�ػ��ϼ۱仯��֪��Ԫ�ػ��ϼ۽���Ϊ-3�ۣ���Ԫ�ػ��ϼ�����Ϊ+1�ۣ����Ե�Ԫ�صķǽ�����ǿ����Ԫ�أ�
�ʴ�Ϊ��NCl3+3H2O=NH3+3HClO��N��
���������⿼�����������ʵķ����жϣ���Ҫ�ǵ����仯�������ʵ�Ӧ�ã�ע��������ԭ��Ӧ�����غ�ķ����жϣ��������Һ������Ũ�ȴ�С�Ƚϵķ�������ѧ����ʽ��дӦ�ã���Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
��֪A��B��C��D��E�Ƕ�����ԭ�������������������Ԫ�أ�Aԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С��B��Eͬ���壬��E��ԭ��������B��������C��D�ǽ��������ǵ����������������ˮ������˵������ȷ���ǣ�������
| A�������ӵİ뾶��C��D��E��B | B����ҵ�ϳ��õ�ⷨ�Ƶ�C��D�ĵ��� | C���ȶ��ԣ�A2B��A2E | D������D������ұ��ijЩ���۽��� |
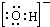
 2DB3����3.2gDB2��ȫת��ΪDB3����ʱ����akJ��1mol DB3������ȫת��Ϊ��ˮ�������bkJ��������33.6L DB2��ȫ�������������Ӧ����
2DB3����3.2gDB2��ȫת��ΪDB3����ʱ����akJ��1mol DB3������ȫת��Ϊ��ˮ�������bkJ��������33.6L DB2��ȫ�������������Ӧ����