题目内容
【题目】氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。
查阅资料:①实验室用饱和NaNO2与NH4Cl溶液共热制N2:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O。
NaCl+N2↑+2H2O。
②工业制氮化铝:Al2O3+3C+N2![]() 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。
③AlN与NaOH饱和溶液反应:AlN+NaOH+H2O![]() NaAlO2+NH3↑。
NaAlO2+NH3↑。
Ⅰ.氮化铝的制备
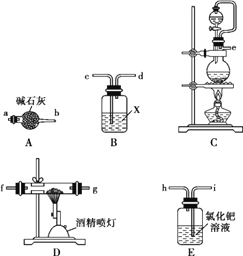
(1)实验中使用的装置如上图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→____________(根据实验需要,上述装置可使用多次)。
(2)B装置内的X液体可能是____;E装置内氯化钯溶液的作用可能是_______。
Ⅱ.氮化铝纯度的测定
【方案ⅰ】甲同学用下图装置测定AlN的纯度(部分夹持装置已略去)。
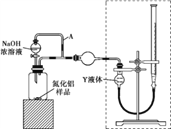
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是____。
a.CCl4 b.H2O c.NH4Cl饱和溶液 d.植物油
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是____ (填“偏大”“偏小”或“不变”)。
【方案ⅱ】乙同学按以下步骤测定样品中AlN的纯度。
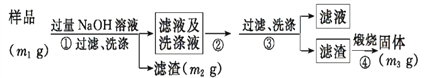
(5)步骤②的操作是_________。
(6)实验室里煅烧滤渣使其分解,除了必要的热源和三脚架以外,还需要的仪器有______等。
(7) 样品中AlN的纯度是__________(用m1、m2、m3表示)。
【答案】 a→b→f(g)→g(f)→a(c)→b(d)→I 浓硫酸 吸收CO,防止污染 ad 偏大 通入过量CO2气体 坩埚、泥三角、坩埚钳 ![]() ×100%
×100%
【解析】(1) 实验室用饱和NaNO2与NH4Cl溶液共热制N2:NaNO2+NH4Cl![]() NaCl+N2↑+2H2O,可以需要装置C制备氮气,生成的氮气中经过干燥后与Al2O3和C在装置D中反应生成AlN和CO,CO会污染空气,可以通过氯化钯溶液吸收,氮化铝在高温下能水解,需要防止外界水蒸气进入装置D,因此按照氮气气流方向,各仪器接口连接顺序为:e→c→d→a→b→f(g)→g(f)→a(c)→b(d)→I,故答案为:a→b→f(g)→g(f)→a(c)→b(d)→I;
NaCl+N2↑+2H2O,可以需要装置C制备氮气,生成的氮气中经过干燥后与Al2O3和C在装置D中反应生成AlN和CO,CO会污染空气,可以通过氯化钯溶液吸收,氮化铝在高温下能水解,需要防止外界水蒸气进入装置D,因此按照氮气气流方向,各仪器接口连接顺序为:e→c→d→a→b→f(g)→g(f)→a(c)→b(d)→I,故答案为:a→b→f(g)→g(f)→a(c)→b(d)→I;
(2)根据上述分析,B装置内的X液体可以是浓硫酸;E装置内氯化钯溶液是用来吸收CO,防止污染,故答案为:浓硫酸;吸收CO,防止污染;
(3) AlN+NaOH+H2O= NaAlO2+NH3↑,量气装置中收集的气体为氨气。a.氨气是极性分子,难溶于CCl4,可以选用;b.氨气极易溶于水,不能选用;c.氨气在NH4Cl饱和溶液中溶解度仍然很大,不能选用;d.氨气难溶于植物油,可以选用;故选ad;
(4)若装置中分液漏斗与导气管之间没有导管A连通,,应用氢氧化钠溶液体积的影响会使得测得的氨气的体积偏大,所测AlN纯度偏大,故答案为:偏大;
(5)根据流程图,滤液即洗涤液中含有NaAlO2,经过步骤②得到沉淀为氢氧化铝,因此步骤②是通入过量CO2气体,故答案为:通入过量CO2气体;
(6)实验室里煅烧滤渣氢氧化铝使其分解,除了必要的热源和三脚架以外,还需要的仪器有坩埚、泥三角、坩埚钳,故答案为:坩埚、泥三角、坩埚钳;
(7)根据Al2O3+3C+N2![]() 2AlN+3CO,AlN+NaOH+H2O= NaAlO2+NH3↑,样品的主要成分为Al2O3、C和 AlN,滤渣为C,最终的固体为Al2O3,因此由AlN反应得到的氧化铝的质量为m3-m1+m2,根据铝元素守恒,AlN的质量为
2AlN+3CO,AlN+NaOH+H2O= NaAlO2+NH3↑,样品的主要成分为Al2O3、C和 AlN,滤渣为C,最终的固体为Al2O3,因此由AlN反应得到的氧化铝的质量为m3-m1+m2,根据铝元素守恒,AlN的质量为![]() ×2×41g/mol=
×2×41g/mol=![]() g,样品中AlN的纯度为
g,样品中AlN的纯度为![]() ×100%,故答案为:
×100%,故答案为: ![]() ×100%。
×100%。