题目内容
(15分)某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液。
请根据实验回答问题:
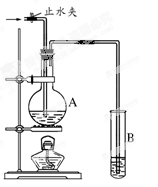
(1)首先根据下图所示,组装实验装置,并在加入试剂前先进行 操作。

(2)烧杯中用NaOH溶液吸收的物质是
(填化学式),利用倒置的漏斗而不是将导气管直接伸入烧杯中的目的是: 。
(3)加热烧瓶20分钟,烧瓶中发生反应的化学方程式是: 。待烧瓶中反应基本结束,撤去酒精灯,利用烧瓶中的余热使反应进行完全。然后由导管a通入足量的空气,以确保烧瓶中的SO2气体全部进入烧杯中。在该实验装置中的 (填仪器名称)起到了确保硫酸溶液体积保持不变的作用。
(4)将充分反应后的烧杯取下,向其中加入足量的双氧水,再加入足量的BaCl2溶液,再进行 、 、 后称量固体的质量为13.98g,请计算能与铜反应的硫酸的最低浓度是 。
(5)有同学提出在上面⑷中可以不必加入双氧水,直接进行后面的实验,也能得到准确的数据,请结合你的理解分析 (填“需要”或“不需要”)加入双氧水,说明原因: 。
请根据实验回答问题:
(1)首先根据下图所示,组装实验装置,并在加入试剂前先进行 操作。

(2)烧杯中用NaOH溶液吸收的物质是
(填化学式),利用倒置的漏斗而不是将导气管直接伸入烧杯中的目的是: 。
(3)加热烧瓶20分钟,烧瓶中发生反应的化学方程式是: 。待烧瓶中反应基本结束,撤去酒精灯,利用烧瓶中的余热使反应进行完全。然后由导管a通入足量的空气,以确保烧瓶中的SO2气体全部进入烧杯中。在该实验装置中的 (填仪器名称)起到了确保硫酸溶液体积保持不变的作用。
(4)将充分反应后的烧杯取下,向其中加入足量的双氧水,再加入足量的BaCl2溶液,再进行 、 、 后称量固体的质量为13.98g,请计算能与铜反应的硫酸的最低浓度是 。
(5)有同学提出在上面⑷中可以不必加入双氧水,直接进行后面的实验,也能得到准确的数据,请结合你的理解分析 (填“需要”或“不需要”)加入双氧水,说明原因: 。
|
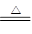 CuSO4+SO2↑+2H2O ( 2分) 长导管(1分)
CuSO4+SO2↑+2H2O ( 2分) 长导管(1分)⑷过滤、洗涤、干燥 (共3分) 12mol/L ( 2分)
⑸需要 ( 2分) 原因:在烧杯中生成的Na2SO3可能被部分氧化为Na2SO4,如果不加入双氧水而直接测定沉淀质量则无法确定S元素的物质的量,从而使实验结果错误。(2分)
(1)组装装置之后,不能立即装入试剂,二应该是首先检验装置气密性。
(2)SO2属于大气污染物,需要尾气处理。由于SO2易溶于水,如果导管口直接插入溶液中,容易导致液体倒流,所以倒置的漏斗起防倒吸作用。
(3)在加热的条件下,浓硫酸能氧化单质铜,方程式为Cu+2H2SO4(浓)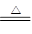 CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。
CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。
(4)加入双氧水是氧化亚硫酸钠的。加入氯化钡能产生硫酸钡沉淀,所以需要通过过滤、洗涤、干燥操作。硫酸钡是13.98g,物质的量是13.98g÷233g/mol=0.06mol,则参加反应的硫酸0.12mol,所以剩余硫酸是18mol/L×0.02L-0.12mol=0.24mol,浓度是0.24mol÷0.02L=12mol/L。即能与铜反应的硫酸的最低浓度是12mol/L。
(5)由于亚硫酸钠不稳定,易被氧化生成硫酸钠,所以如果不加入双氧水而直接测定沉淀质量则无法确定S元素的物质的量,从而使实验结果错误,因此必须加入双氧水。
(2)SO2属于大气污染物,需要尾气处理。由于SO2易溶于水,如果导管口直接插入溶液中,容易导致液体倒流,所以倒置的漏斗起防倒吸作用。
(3)在加热的条件下,浓硫酸能氧化单质铜,方程式为Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。
CuSO4+SO2↑+2H2O。再加热的条件下,水蒸气易挥发,所以利用长导管,起冷凝回流作用。(4)加入双氧水是氧化亚硫酸钠的。加入氯化钡能产生硫酸钡沉淀,所以需要通过过滤、洗涤、干燥操作。硫酸钡是13.98g,物质的量是13.98g÷233g/mol=0.06mol,则参加反应的硫酸0.12mol,所以剩余硫酸是18mol/L×0.02L-0.12mol=0.24mol,浓度是0.24mol÷0.02L=12mol/L。即能与铜反应的硫酸的最低浓度是12mol/L。
(5)由于亚硫酸钠不稳定,易被氧化生成硫酸钠,所以如果不加入双氧水而直接测定沉淀质量则无法确定S元素的物质的量,从而使实验结果错误,因此必须加入双氧水。

练习册系列答案
相关题目