题目内容
3.100ml0.25mol•L-1 AlCl3溶液中,Cl-的物质的量浓度为0.75 mol•L-1;若将上述溶液加水稀释到500ml,Cl-的物质的量浓度为0.15 mol•L-1.分析 溶液中离子的浓度=电解质的浓度×一个分子中含有的离子数目,据此计算出氯离子的物质的量浓度;根据稀释前后离子的浓度不变计算出稀释后Cl-的物质的量浓度.
解答 解:100ml0.25mol•L-1 AlCl3溶液中,Cl-的物质的量浓度为c(Cl-)=3c(AlCl3)=3×0.25mol/L=0.75mol/L;
设稀释后溶液中Cl-的物质的量浓度为c,则:0.75mol/L×0.1L=c×0.5L,解得c=0.15mol/L,
故答案为:0.75;0.15.
点评 本题考查物质的量浓度有关计算,题目难度不大,明确离子浓度与电解质的浓度、组成的关系为解答关键,注意溶液稀释前后溶质的物质的量不变.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
13.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1L0.1mol•L-1FeCl3溶液中含有的Fe3+离子数目为0.1NA | |
| B. | 常温常压下,4.6gNO2和N2O4混合物中含有的原子总数为0.3NA | |
| C. | 1mol (环己烷)中含有6NA共价键 (环己烷)中含有6NA共价键 | |
| D. | 常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1NA |
11.下列有关化学用语表示正确的是( )
| A. | “碳铵”的化学式:(NH4)2CO3 | |
| B. | 二氧化碳的结构式:O=C=O | |
| C. | 钾原子的结构示意图: | |
| D. | 中子数为138、质子数为88的镭(Ra)原子:${\;}_{88}^{138}$Ra |
18.下列物质不含有氧元素的是( )
| A. | 氯酸钾 | B. | 氯化钾 | C. | 次氯酸 | D. | 空气 |
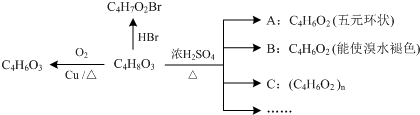
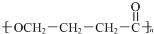 .
.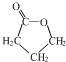 +H2O.
+H2O. .
.