题目内容
【题目】聚合氯化铝([Al2( OH)nCl6-n]m}是一种新型高效净水剂,与一般絮凝剂相比,它的吸附能力强、絮凝率高,可由AlCl3经水解法制得。回答下列问题:
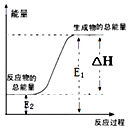
(1)工业上可用Cl2、Al2O3和焦炭在高温下反应制取AlCl3![]()
已知:4Al(s)+3O2(g)=2Al2O3(s) △H1
2C(s)+O2(g)=2CO(g) △H2
2Al(s)+3Cl2(g)=2A1Cl3(g) △H3
①Al2O3(s)+3C(s)+3Cl2(g) ![]() 2AlCl3(g)+3CO(g) △H=____________________。
2AlCl3(g)+3CO(g) △H=____________________。
②反应3A12O3(s)+6Cl2(g) ![]() 4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是_________________________________。
4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是_________________________________。
(2)AlCl3在水溶液中分三步水解
Al3++H2O![]() Al(OH)2++H+ K1
Al(OH)2++H+ K1
Al(OH)2++H2O![]() Al(OH)2++H+ K2
Al(OH)2++H+ K2
Al(OH)2++ H2O![]() Al(OH)3+H+ K3
Al(OH)3+H+ K3
①K1、K2、K3由小到大的顺序是_______________________。
②控制溶液的pH在一定范围内,上述水解产物才能聚合生成聚合氯化铝。pH偏小时,Al3+的水解程度弱;pH偏大时的影响是___________________________。
(3)已知有如下可逆反应: ![]()
![]()
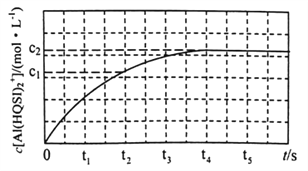
298K时,将1mL 1 mol·L-1 AlCl3溶液与1mL2 a mol ·L-1H2QSI溶液混合发生上述反应,溶液中c[Al(HQSI)2+]与时间(t)的关系如图所示。
①下列可判断该反应达到平衡状态的是______________(填标号)。![]()
A.溶液的pH不再变化 B. v(Al3+)=v [Al(HQSI)2+]
C.溶液颜色不再变化 D.c(A13+)/c(H2QSI)不再变化
②0~t2时间内,该反应的平均反应速率v(H2QSI)= _________________。
③298K时,该反应的平衡常数K=_________________。
(4)该方法制得的聚合氯化铝的优点是不含其它金属离子,但盐基度低(盐基度:衡量絮凝剂絮凝效果的重要指标,定义式为:盐基度=n(OH)/3n(Al),n为物质的量)。常温下实验测量样品的盐基度,取m g样品,该样品中Al的质量分数为w;加入煮沸后冷却的蒸馏水溶解,配成1L溶液,测得该溶液pH=9.0。则其盐基度为________________。
【答案】 ![]() △H2+△H3-
△H2+△H3-![]() △H1 焦炭与O2反应,降低O2的浓度,导致反应不断地向正反应方向进行 K3<K2<K1(1分) 形成氢氧化铝沉淀 A、C; 2c1/t2 mol/(L·s)
△H1 焦炭与O2反应,降低O2的浓度,导致反应不断地向正反应方向进行 K3<K2<K1(1分) 形成氢氧化铝沉淀 A、C; 2c1/t2 mol/(L·s) 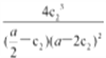
![]() )
)
【解析】(1)已知:Ⅰ4Al(s)+3O2(g)=2Al2O3(s) △H1
Ⅱ2C(s)+O2(g)=2CO(g) △H2
Ⅲ2Al(s)+3Cl2(g)=2A1Cl3(g) △H3
根据盖斯定律,由![]() 得反应①Al2O3(s)+3C(s)+3Cl2(g)
得反应①Al2O3(s)+3C(s)+3Cl2(g) ![]() 2AlCl3(g)+3CO(g) △H=
2AlCl3(g)+3CO(g) △H=![]() △H2+△H3-
△H2+△H3-![]() △H1;②反应3A12O3(s)+6Cl2(g)
△H1;②反应3A12O3(s)+6Cl2(g) ![]() 4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是焦炭与O2反应,降低O2的浓度,导致反应不断地向正反应方向进行;(2) ①盐类的水解分步进行且水解程度逐步减弱,故K1、K2、K3由小到大的顺序是K3<K2<K1;②pH偏大时Al3+水解形成氢氧化铝沉淀;(3) A.根据反应
4AlCl3(g)+3O2(g)在高温下较难发生,但加入焦炭后可提高氯气的转化率,原因是焦炭与O2反应,降低O2的浓度,导致反应不断地向正反应方向进行;(2) ①盐类的水解分步进行且水解程度逐步减弱,故K1、K2、K3由小到大的顺序是K3<K2<K1;②pH偏大时Al3+水解形成氢氧化铝沉淀;(3) A.根据反应![]() ,溶液的pH不再变化,氢离子浓度不再变化,则反应达平衡状态,选项A正确;B. v(Al3+)=v [Al(HQSI)2+],没有说明是正反应速率还是逆反应速率,不能确定正逆反应速率相等,不一定达平衡状态,选项B错误;C.反应中只有Al(HQSI)2+为有色配合物,溶液颜色不再变化,说明各浓度保持不变,反应达平衡状态,选项C正确;D.开始投料比1:2与反应计量数相等,故反应后c(A13+)/c(H2QSI)保持1:2,故比值不再变化不能说明反应达平衡,选项D错误。答案选AC;②由图中信息可知,0~t2时间内,该反应的平均反应速率v(H2QSI)=2 v[Al(HQSI)2+]=
,溶液的pH不再变化,氢离子浓度不再变化,则反应达平衡状态,选项A正确;B. v(Al3+)=v [Al(HQSI)2+],没有说明是正反应速率还是逆反应速率,不能确定正逆反应速率相等,不一定达平衡状态,选项B错误;C.反应中只有Al(HQSI)2+为有色配合物,溶液颜色不再变化,说明各浓度保持不变,反应达平衡状态,选项C正确;D.开始投料比1:2与反应计量数相等,故反应后c(A13+)/c(H2QSI)保持1:2,故比值不再变化不能说明反应达平衡,选项D错误。答案选AC;②由图中信息可知,0~t2时间内,该反应的平均反应速率v(H2QSI)=2 v[Al(HQSI)2+]=![]() mol/(L·s);③298K时,将1 mol ·L-1 AlCl3溶液与1mL2a mol ·L-1H2QSI溶液混合发生上述反应,达平衡时c(A13+)=(
mol/(L·s);③298K时,将1 mol ·L-1 AlCl3溶液与1mL2a mol ·L-1H2QSI溶液混合发生上述反应,达平衡时c(A13+)=(![]() ,c(H2QSI)= (
,c(H2QSI)= (![]() ,c[Al(HQSI)2+]=
,c[Al(HQSI)2+]=![]() ,c(H+)=
,c(H+)=![]() ,反应的平衡常数K=
,反应的平衡常数K=![]() ;(4)配成1L溶液,pH=9.0。则c(OHˉ)=10-5mol/L,其盐基度为n(OH)/3n(Al)=
;(4)配成1L溶液,pH=9.0。则c(OHˉ)=10-5mol/L,其盐基度为n(OH)/3n(Al)=![]() =
=![]() 。
。