题目内容
过氧化钠能与二氧化碳反应,在“神七”的航天舱中、在宇航员太空漫步时穿的航天服中、在潜艇中均使用过氧化钠作制氧剂,供人呼吸之用。某学生选用大理石、盐酸和一定量过氧化钠药品设计实验,验证这一事实。
请根据所给装置回答下列问题: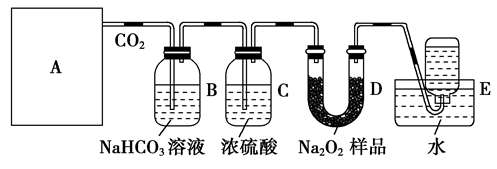
(1)A是制取CO2的装置,最好选用下列装置中的________(填序号)。
(2)B装置中发生的离子方程式是_____________________________________________。
C装置的作用是_____________________________________________________。
(3)D装置中发生反应的化学方程式是______________________________________。
(4)要想得到较纯净的氧气,可在装置D和E之间增加一盛有__ ______(填写试剂名称)的________(填写装置名称)。
(5)如何检验集气瓶中收集到的气体_______________________________。
(1)③ (2)HCO3-+H+=H2O+CO2↑ 除去CO2中混有的水蒸气
(3)2Na2O2+2CO2=2Na2CO3+O2
(4)碱石灰 干燥管或U形管(或NaOH溶液 洗气瓶)
(5)将带火星的木条伸入集气瓶中,木条复燃
解析试题分析:(1)制取CO2用大理石和盐酸,属于“固+液不加热型”制取气体,因此装置选用③。(2)制取CO2用的盐酸有挥发性,所以在制取的二氧化碳气体中含有氯化氢气体。用碳酸氢钠溶液来除去氯化氢又不消耗二氧化碳气体。反应的离子方程式是:HCO3-+H+=H2O+CO2↑这时的二氧化碳气体中还含有水蒸气。可以利用浓硫酸的吸水性来除去。(3)在D装置中二氧化碳与过氧化钠发生反应:2Na2O2+2CO2=2Na2CO3+O2(4)为了除去未完全反应的二氧化碳气体杂质,得到纯净的氧气,可在装置D和E之间增加一个装置,内盛有能与二氧化碳发生反应又不与氧气反应的固体物质。一般用碱石灰或熟石灰,盛放在干燥管中。(5)检验O2,一般用带火星的木条。将带火星的木条伸入集气瓶口,木条复燃证明该气体是氧气。
考点:考查过氧化钠的用途及二氧化碳的实验室制法、除杂、干燥、氧气的检验等知识。

某小组取一定质量的FeSO4固体,利用下图装置进行实验。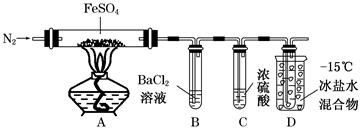
| 实验 | 实验过程 | 实现现象 |
| ① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
| ③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
| ④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8 ℃。
(1)实验③反应的离子方程式是_____________________________________________。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有________气体,依据是____________________________________________________
(3)实验④反应的离子方程式是_____________________________________________。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:____________________________________________(用必要的文字和化学方程式解释)。
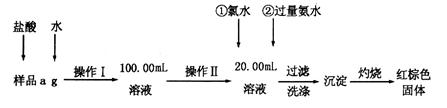
为测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,称取一定质量的样品,甲同学利用图I所示装置测量产生CO2的体积,乙同学利用图II所示装置通过干燥管的增重测量产生CO2的质量,已知所用稀硫酸均足量。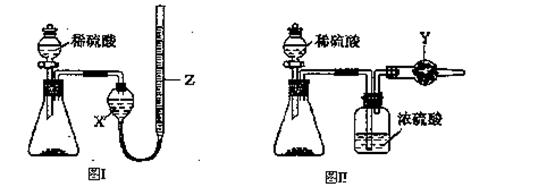
(l)盛放稀硫酸的仪器名称为 ;
(2)试剂X为 ,试剂Y为 ;
(3)甲同学在进行实验时,为减小误差,应注意的事项有(填选项字母) ;
| A.读数前应使整套装置冷却至室温 |
| B.调整Z的高度使量气装置左右液面相平 |
| C.读数时视线与Z内凹液面最低点相切 |
| D.读数前应通入一定量的N2使生成的CO2全部进入量气装置 |
铁铜单质及其化合物的应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯: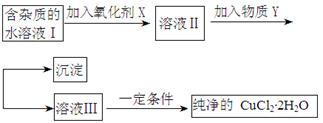
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂的目的是
(2)下列最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是
(4)如果不用物质Y而直接用可溶性碱溶液能不能达到目的? (填“能”或者“不能”)。若不能,试解释原因 (若填“能”,此空不用回答)
(5)最后能不能直接蒸发得到CuCl2·2H2O? (填“能”或者“不能”)。若不能,应该如何操作才能得到CuCl2·2H2O (若填“能”,此空不用回答)
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
(7)若向溶液Ⅱ中加入镁粉,产生的气体是 ,试解释原因
(8)FeCl3溶液具有净水作用的原因是
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
I、经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下: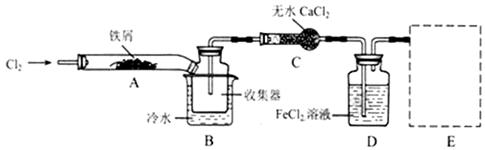
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为 。
(2)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号) 。
(3)如果没有装置C的设计,会导致
(4)用离子方程式表示虚线框E中所增加装置和试剂的作用: 。
(5)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,请写出反应的离子方程式: 。
Ⅱ、反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③ 。
为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| ①取少量所得溶液于试管中,加入少量KSCN溶液。 | _________________。 | 说明:假设②不成立,假设①或③成立;反应的离子方程式是_____________。 |
| ②另取少量所得溶液于试管中,加入少量酸性 KMnO4溶液。 | 溶液紫红色退去 | 说明:________________________。 |
综合上述实验分析,所得溶液中含有的金属阳离子有 。
青石棉(cricidolite)是一种致癌物质,是《鹿特丹公约》中受限制的46种化学品之一,其化学式为Na2Fe5Si8O22(OH)2.青石棉用稀硝酸溶液处理时,还原产物只有NO,下列说法不正确的是( )
| A.青石棉是一种硅酸盐产品 |
| B.青石棉中含有一定量的石英晶体 |
| C.青石棉的化学组成可表示为:Na2O·3FeO·Fe2O3·8SiO2·H2O |
| D.1 mol青石棉能使1 mol HNO3被还原 |
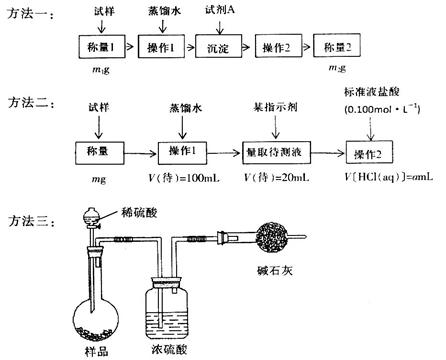

 MgO+H2↑ Mg3N2 +6H2O =3Mg(OH)2+2NH3↑
MgO+H2↑ Mg3N2 +6H2O =3Mg(OH)2+2NH3↑