题目内容
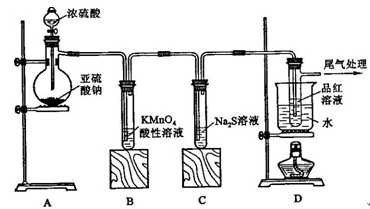
下图表示在没有通风橱的条件下制备氯气时设计的装置,图中a、b是可控制的弹簧铁夹。(氯气在饱和氯化钠溶液中的溶解度较小。)
(1)仪器A的名称是 ;水槽中应盛放的是 ;烧杯中盛放的是 ;烧瓶中反应的化学方程式 ;
在收集氯气时,应打开 关闭 (填a, b)当氯气收集完毕,尾气处理时烧杯中发生反应的离子方程式 。
(1)分液漏斗 饱和食盐水 氢氧化钠溶液
4HCl(浓)+MnO2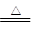 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)a b Cl2 + 2OH-=Cl- + ClO- + H2O
解析试题分析:(1)根据仪器特点可知A为分液漏斗;根据信息氯气在饱和氯化钠溶液中的溶解度较小,实验室常用排饱和食盐水法收集氯气;实验室常用二氧化锰和浓盐酸在加热条件下制取氯气,化学方程式为4HCl(浓)+MnO2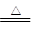 MnCl2+Cl2↑+2H2O;(2)根据题给装置图分析,收集氯气时,应关闭b,打开a;收集完毕,关闭a,打开b,多余的气体通入氢氧化钠溶液进行吸收,防止污染空气,离子方程式为Cl2 + 2OH-=Cl- + ClO- + H2O。
MnCl2+Cl2↑+2H2O;(2)根据题给装置图分析,收集氯气时,应关闭b,打开a;收集完毕,关闭a,打开b,多余的气体通入氢氧化钠溶液进行吸收,防止污染空气,离子方程式为Cl2 + 2OH-=Cl- + ClO- + H2O。
考点:考查氯气的实验室制法

 名校课堂系列答案
名校课堂系列答案“蛇纹石石棉”主要成分有二氧化硅、氧化镁和结晶水,它的化学式是Mg6[(OH)4Si2O5]2。
(1)“蛇纹石石棉”的氧化物形式为______________________,其中原子半径最大的元素
在周期表中的位置是______________________。
(2)Si原子的最外层的电子排布式为_____________,SiO2与NaOH溶液反应的化学方程式
为________________________________________________。
(3) SiCl4比SiO2的熔点_____(填“低”、“高”),原因是__________________________。
(4)从哪些方面不能判断Si和O的非金属性强弱 。
| A.利用Si和O在周期表中的位置 |
| B.SiO2与水不发生反应 |
| C.Si在一定条件下与氧气反应,生成SiO2 |
| D.H2SiO3的酸性比H2O的酸性强 |
硫元素有多种化合价,可形成多种化合物。
(1)常温下用1 mol·L﹣1 100 mL NaOH溶液恰好完全吸收0.1 mol SO2气体,此反应的离子方程式为 ;该溶液pH_______7(填“=”“>”或“<”)。
(2)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
实验①可说明________(填字母)
| A.该Na2S2O3溶液中水电离的c(OH﹣)=10﹣8mol/L |
| B.H2S2O3是一种弱酸 |
| C.Na2S2O3是一种弱电解质 |
| D.Na2S2O3水解方程式为S2O32﹣+2H2O=H2S2O3+2OH﹣ |
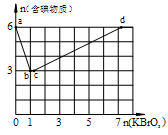
(3)实验室制得的Na2S2O3粗晶体中往往含有少量杂质。为了测定粗产品中Na2S2O3·5H2O(摩尔质量为248g/mol)的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定粗产品中杂质与酸性KMnO4溶液不反应)。称取1.28 g的粗样品溶于水,用0.40mol/L KMnO4溶液(加入适量硫酸酸化)滴定,当溶液中S2O32﹣全部被氧化时,消耗KMnO4溶液体积20.00 mL。(已知:5S2O32﹣+8MnO4﹣+14H+=8Mn2++10SO42﹣+7H2O)。
试回答:
①KMnO4溶液置于——(填“酸式”或“碱式”)滴定管中,滴定终点的现象为 。
②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3·5H2O的质量分数的测量结果_____________(填“偏高”“偏低”或“不变”)。
③产品中Na2S2O3·5H2O的质量分数为 。

 MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
 2NO
2NO CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O